তরল জলের ত্রিমাত্রিক অবস্থা অধ্যয়ন করা কঠিন, তবে বরফের স্ফটিকগুলির গঠন বিশ্লেষণ করে অনেক কিছু শিখেছে। চারটি প্রতিবেশী হাইড্রোজেন-ইন্টার্যাক্টিং অক্সিজেন পরমাণু একটি টেট্রাহেড্রনের শীর্ষবিন্দু (টেট্রা=চার, হেড্রন=সমতল) দখল করে। বরফের মধ্যে এই ধরনের বন্ধন ভাঙতে গড় শক্তির প্রয়োজন অনুমান করা হয় 23 kJ/mol-1.

> যখন এটি গলে যায়, এটি তরল জল দ্বারা ধারণ করা হয়, যার গঠনটি অনিয়মিত। হাইড্রোজেন বন্ধন অধিকাংশ বিকৃত হয়. হাইড্রোজেন-বন্ধনযুক্ত বরফের স্ফটিক জালি ভাঙতে তাপের আকারে প্রচুর পরিমাণে শক্তি লাগে।
বরফের চেহারার বৈশিষ্ট্য (Ih)
অনেক বাসিন্দারা ভাবছেন কি ধরনের স্ফটিক জালি বরফ আছে। প্রয়োজনীয়এটি লক্ষ করা উচিত যে বেশিরভাগ পদার্থের ঘনত্ব হিমাঙ্কের সময় বৃদ্ধি পায়, যখন আণবিক গতিবিধি ধীর হয়ে যায় এবং ঘনভাবে প্যাক করা স্ফটিক তৈরি হয়। পানির ঘনত্বও বৃদ্ধি পায় কারণ এটি সর্বোচ্চ 4°C (277K) এ শীতল হয়। তারপর, যখন তাপমাত্রা এই মানের নিচে নেমে আসে, তখন তা প্রসারিত হয়।
এই বৃদ্ধি একটি উন্মুক্ত, হাইড্রোজেন-বন্ধনযুক্ত বরফের স্ফটিক তৈরির কারণে হয়েছে যার জালি এবং নিম্ন ঘনত্ব রয়েছে, যেখানে প্রতিটি জলের অণু উপরোক্ত উপাদান এবং অন্যান্য চারটি মান দ্বারা দৃঢ়ভাবে আবদ্ধ থাকে, যখন যথেষ্ট দ্রুত গতিতে চলে আরো ভর আছে. যেহেতু এই ক্রিয়াটি ঘটে, তরলটি উপরে থেকে নীচের দিকে জমে যায়। এটির গুরুত্বপূর্ণ জৈবিক ফলাফল রয়েছে, যার ফলস্বরূপ পুকুরের উপর বরফের স্তরটি জীবন্ত প্রাণীদের প্রচণ্ড ঠান্ডা থেকে দূরে রাখে। উপরন্তু, জলের দুটি অতিরিক্ত বৈশিষ্ট্য এর হাইড্রোজেন বৈশিষ্ট্যের সাথে সম্পর্কিত: নির্দিষ্ট তাপ এবং বাষ্পীভবন।
কাঠামোর বিশদ বিবরণ
প্রথম মানদণ্ড হল একটি পদার্থের 1 গ্রামের তাপমাত্রা 1 ডিগ্রি সেলসিয়াস বাড়ানোর জন্য প্রয়োজনীয় পরিমাণ। পানির ডিগ্রী বাড়ানোর জন্য তুলনামূলকভাবে প্রচুর পরিমাণে তাপের প্রয়োজন হয় কারণ প্রতিটি অণু অসংখ্য হাইড্রোজেন বন্ধনের সাথে জড়িত যা গতিশক্তি বৃদ্ধির জন্য অবশ্যই ভাঙতে হবে। যাইহোক, সমস্ত বৃহৎ বহুকোষী জীবের কোষ এবং টিস্যুতে H2O এর প্রাচুর্যের মানে হল যে কোষের অভ্যন্তরে তাপমাত্রার ওঠানামা কম করা হয়। এই বৈশিষ্ট্যটি অত্যন্ত গুরুত্বপূর্ণ, যেহেতু বেশিরভাগ জৈব রাসায়নিক বিক্রিয়ার হারসংবেদনশীল।
জলের বাষ্পীভবনের তাপও অন্যান্য অনেক তরলের তুলনায় উল্লেখযোগ্যভাবে বেশি। এই দেহকে গ্যাসে রূপান্তর করতে প্রচুর পরিমাণে তাপের প্রয়োজন হয়, কারণ জলের অণুগুলি একে অপরের থেকে স্থানচ্যুত হতে এবং উল্লিখিত পর্যায়ে প্রবেশ করার জন্য হাইড্রোজেন বন্ধনগুলিকে অবশ্যই ভাঙতে হবে। পরিবর্তনযোগ্য দেহগুলি স্থায়ী ডাইপোল এবং অন্যান্য অনুরূপ যৌগগুলির সাথে যোগাযোগ করতে পারে এবং যেগুলি আয়নিত এবং দ্রবীভূত হয়৷
উপরে উল্লিখিত অন্যান্য পদার্থের সংস্পর্শে আসতে পারে শুধুমাত্র যদি পোলারিটি থাকে। এই যৌগই এই উপাদানগুলির গঠনের সাথে জড়িত। উপরন্তু, এটি ইলেক্ট্রোলাইট থেকে গঠিত এই কণাগুলির চারপাশে সারিবদ্ধ হতে পারে, যাতে জলের অণুর নেতিবাচক অক্সিজেন পরমাণুগুলি ক্যাটেশনের দিকে থাকে এবং ধনাত্মক আয়ন এবং হাইড্রোজেন পরমাণুগুলি অ্যানিয়নের দিকে থাকে৷
কঠিন পদার্থে, একটি নিয়ম হিসাবে, আণবিক স্ফটিক জালি এবং পারমাণবিকগুলি গঠিত হয়। অর্থাৎ, যদি আয়োডিন এমনভাবে তৈরি করা হয় যাতে এতে I2, থাকে, তাহলে কঠিন কার্বন ডাই অক্সাইডে অর্থাৎ শুষ্ক বরফে CO2 অণু থাকে স্ফটিক জালি নোড এ অবস্থিত. অনুরূপ পদার্থের সাথে মিথস্ক্রিয়া করার সময়, বরফের একটি আয়নিক স্ফটিক জালি থাকে। উদাহরণস্বরূপ, গ্রাফাইট, যার কার্বনের উপর ভিত্তি করে একটি পারমাণবিক কাঠামো রয়েছে, এটি হীরার মতো পরিবর্তন করতে সক্ষম নয়৷
যখন টেবিল লবণের একটি স্ফটিক পানিতে দ্রবীভূত হয় তখন কী ঘটে: মেরু অণুগুলি স্ফটিকের চার্জযুক্ত উপাদানগুলির প্রতি আকৃষ্ট হয়, যা এর পৃষ্ঠে সোডিয়াম এবং ক্লোরাইডের অনুরূপ কণা তৈরির দিকে পরিচালিত করে, যার ফলে এই দেহগুলি তৈরি হয়একে অপরের থেকে স্থানচ্যুত হয়, এবং এটি দ্রবীভূত হতে শুরু করে। এখান থেকে এটি লক্ষ্য করা যায় যে বরফের আয়নিক বন্ধন সহ একটি স্ফটিক জালি রয়েছে। প্রতিটি দ্রবীভূত Na + বেশ কয়েকটি জলের অণুর ঋণাত্মক প্রান্তকে আকর্ষণ করে, যখন প্রতিটি দ্রবীভূত Cl - ধনাত্মক প্রান্তকে আকর্ষণ করে। প্রতিটি আয়নের চারপাশের শেলকে বলা হয় এস্কেপ গোলক এবং এতে সাধারণত দ্রাবক কণার কয়েকটি স্তর থাকে।
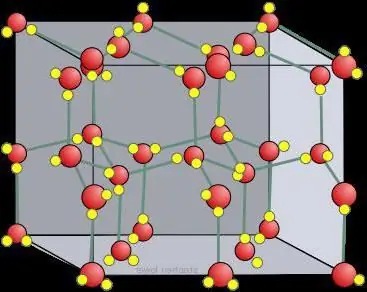
শুকনো বরফের স্ফটিক জালি
ভেরিয়েবল বা উপাদান দ্বারা বেষ্টিত একটি আয়নকে সালফেটেড বলা হয়। যখন দ্রাবক জল হয়, এই ধরনের কণা হাইড্রেটেড হয়। এইভাবে, যে কোনও মেরু অণু তরল দেহের উপাদানগুলির দ্বারা সমাধান করা হয়। শুষ্ক বরফে, স্ফটিক জালির ধরন একত্রিত অবস্থায় পারমাণবিক বন্ধন গঠন করে, যা অপরিবর্তিত থাকে। আরেকটি জিনিস হল স্ফটিক বরফ (হিমায়িত জল)। আয়নিক জৈব যৌগ যেমন কার্বক্সিলেজ এবং প্রোটোনেটেড অ্যামাইনগুলি অবশ্যই হাইড্রক্সিল এবং কার্বনাইল গ্রুপে দ্রবণীয় হতে হবে। এই ধরনের কাঠামোর মধ্যে থাকা কণাগুলি অণুর মধ্যে স্থানান্তরিত হয় এবং তাদের মেরু সিস্টেমগুলি এই শরীরের সাথে হাইড্রোজেন বন্ধন তৈরি করে।
অবশ্যই, একটি অণুতে শেষ নির্দেশিত গোষ্ঠীর সংখ্যা তার দ্রবণীয়তাকে প্রভাবিত করে, যা উপাদানের বিভিন্ন কাঠামোর প্রতিক্রিয়ার উপরও নির্ভর করে: উদাহরণস্বরূপ, এক-, দুই- এবং তিন-কার্বন অ্যালকোহলগুলি মিশ্রিত পানির সাথে, কিন্তু একক হাইড্রোক্সিল যৌগযুক্ত বড় হাইড্রোকার্বন তরলে অনেক কম পাতলা হয়।
ষড়ভুজ Ih আকারে অনুরূপপারমাণবিক স্ফটিক জালি. বরফ এবং পৃথিবীর সমস্ত প্রাকৃতিক তুষার জন্য, এটা ঠিক এই মত দেখায়. এটি জলীয় বাষ্প (অর্থাৎ তুষারকণা) থেকে উত্থিত বরফের স্ফটিক জালির প্রতিসাম্য দ্বারা প্রমাণিত। এটি 194 থেকে স্পেস গ্রুপ P 63/মিমিতে রয়েছে; D 6h, Laue শ্রেণী 6/mm; β- এর অনুরূপ, যার 6টি হেলিকাল অক্ষের একাধিক রয়েছে (এটি বরাবর স্থানান্তর ছাড়াও চারপাশে ঘূর্ণন)। এটির একটি মোটামুটি উন্মুক্ত নিম্ন ঘনত্বের কাঠামো রয়েছে যেখানে সাধারণ কিউবিক (~1/2) বা মুখকেন্দ্রিক ঘনক (~3/4) কাঠামোর তুলনায় দক্ষতা কম (~1/3)৷
সাধারণ বরফের তুলনায়, শুষ্ক বরফের স্ফটিক জালি, CO2 অণু দ্বারা আবদ্ধ, স্থির থাকে এবং শুধুমাত্র পরমাণুর ক্ষয় হলেই পরিবর্তিত হয়৷
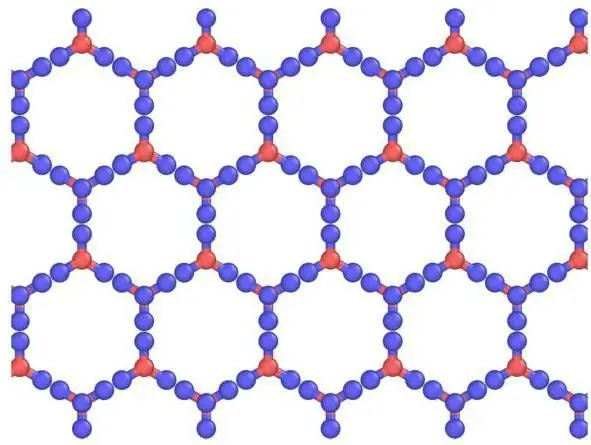
গ্রেটিং এবং তাদের উপাদানের বর্ণনা
ক্রিস্টালগুলিকে স্ফটিক মডেল হিসাবে দেখা যেতে পারে, যার মধ্যে একটির উপরে একটি স্থাপন করা শীট রয়েছে। হাইড্রোজেন বন্ড অর্ডার করা হয়েছে, যদিও বাস্তবে এটি এলোমেলো, যেহেতু প্রোটনগুলি প্রায় 5 K এর উপরে তাপমাত্রায় জল (বরফ) অণুগুলির মধ্যে চলাচল করতে পারে৷ প্রকৃতপক্ষে, এটি সম্ভবত প্রোটনগুলি একটি ধ্রুবক টানেলিং প্রবাহে একটি কোয়ান্টাম তরলের মতো আচরণ করে৷ এটি নিউট্রনের বিক্ষিপ্তকরণ দ্বারা উন্নত হয়, অক্সিজেন পরমাণুর মধ্যে তাদের বিক্ষিপ্ত ঘনত্ব অর্ধেক পথ প্রদর্শন করে, যা স্থানীয়করণ এবং সমন্বিত গতি নির্দেশ করে। এখানে পারমাণবিক, আণবিক স্ফটিক জালির সাথে বরফের মিল রয়েছে।
অণুগুলির হাইড্রোজেন শৃঙ্খলের একটি বিচলিত বিন্যাস রয়েছেসমতলে তার তিন প্রতিবেশীর প্রতি সম্মানের সাথে। চতুর্থ উপাদানটিতে একটি গ্রহনযোগ্য হাইড্রোজেন বন্ড বিন্যাস রয়েছে। নিখুঁত ষড়ভুজ প্রতিসাম্য থেকে একটি সামান্য বিচ্যুতি রয়েছে, কারণ এই শৃঙ্খলের দিকে একক কোষটি 0.3% ছোট। সমস্ত অণু একই আণবিক পরিবেশ অনুভব করে। প্রতিটি "বাক্স" এর ভিতরে আন্তঃস্থায়ী জলের কণা ধরে রাখার জন্য পর্যাপ্ত জায়গা রয়েছে। যদিও সাধারণভাবে বিবেচনা করা হয় না, তারা সম্প্রতি বরফের পাউডারি স্ফটিক জালির নিউট্রন বিচ্ছুরণ দ্বারা কার্যকরভাবে সনাক্ত করা হয়েছে৷
পরিবর্তনশীল পদার্থ
ষড়ভুজাকার দেহে তরল এবং বায়বীয় জল 0.01 ° C, 612 Pa, কঠিন উপাদানগুলির সাথে তিন বিন্দু রয়েছে - তিন -21.985 ° C, 209.9 MPa, এগারো এবং দুই -199.8 ° C, 70 MPa, পাশাপাশি - 34.7 ° C, 212.9 MPa। ষড়ভুজ বরফের অস্তরক ধ্রুবক হল 97.5.
এই উপাদানটির গলে যাওয়া বক্ররেখা MPa দ্বারা দেওয়া হয়। রাষ্ট্রের সমীকরণগুলি পাওয়া যায়, সেগুলি ছাড়াও, ষড়ভুজ বরফের তাপমাত্রা এবং এর জলীয় সাসপেনশনের সাথে ভৌত বৈশিষ্ট্যের পরিবর্তন সম্পর্কিত কিছু সাধারণ অসমতা। কঠোরতা ওঠানামা করে জিপসাম (≦2) থেকে 0°C থেকে ফেল্ডস্পার (6 Mohs) থেকে -80°C তাপমাত্রায়, পরম কঠোরতায় একটি অস্বাভাবিকভাবে বড় পরিবর্তন (> 24 বার)।
বরফের ষড়ভুজ স্ফটিক জালিটি ষড়ভুজ প্লেট এবং কলাম তৈরি করে, যেখানে উপরের এবং নীচের মুখগুলি বেসাল প্লেন {0 0 0 1} যার এনথালপি 5.57 μJ সেমি -2, এবং অন্যান্য সমতুল্য পার্শ্ব অংশগুলিকে 5, 94 সহ প্রিজমের অংশ বলা হয় {1 0 -1 0}µJ সেমি -2। 6.90 ΜJ ˣ cm -2 সহ গৌণ পৃষ্ঠতলগুলি {1 1 -2 0} কাঠামোর পার্শ্ব দ্বারা গঠিত সমতলগুলির সাথে গঠিত হতে পারে৷
এই ধরনের কাঠামো ক্রমবর্ধমান চাপের সাথে তাপ পরিবাহিতার একটি অস্বাভাবিক হ্রাস দেখায় (পাশাপাশি কম ঘনত্বের ঘন এবং নিরাকার বরফ), তবে বেশিরভাগ স্ফটিক থেকে আলাদা। এটি হাইড্রোজেন বন্ডের পরিবর্তনের কারণে, যা বরফ এবং জলের স্ফটিক জালিতে শব্দের অনুপ্রস্থ গতিকে হ্রাস করে৷
বড় স্ফটিক নমুনা এবং যে কোনও পছন্দসই বরফের পৃষ্ঠ কীভাবে প্রস্তুত করা যায় তা বর্ণনা করার পদ্ধতি রয়েছে। এটা অনুমান করা হয় যে অধ্যয়নের অধীনে ষড়ভুজাকার শরীরের পৃষ্ঠের হাইড্রোজেন বন্ধন বাল্ক সিস্টেমের ভিতরের চেয়ে বেশি অর্ডার করা হবে। ফেজ-ল্যাটিস ফ্রিকোয়েন্সি জেনারেশন সহ ভেরিয়েশনাল স্পেকট্রোস্কোপি দেখিয়েছে যে ষড়ভুজ বরফের বেসাল পৃষ্ঠের সাবসারফেস HO চেইনে দুটি উপরের স্তরের (L1 এবং L2) মধ্যে একটি কাঠামোগত অসমতা রয়েছে। ষড়ভুজগুলির উপরের স্তরগুলিতে গৃহীত হাইড্রোজেন বন্ধনগুলি (L1 O ··· HO L2) উপরের সঞ্চয় (L1 OH ··· O L2) থেকে দ্বিতীয় স্তরে গৃহীত হওয়াগুলির চেয়ে শক্তিশালী। ইন্টারেক্টিভ ষড়ভুজ বরফ কাঠামো উপলব্ধ।
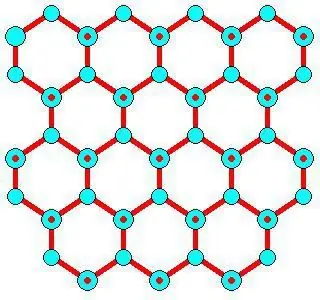
উন্নয়ন বৈশিষ্ট্য
বরফ গঠনের জন্য ন্যূনতম সংখ্যক জলের অণু প্রয়োজন আনুমানিক 275 ± 25, একটি সম্পূর্ণ 280 আইকোসেহেড্রাল ক্লাস্টারের জন্য। গঠনটি 10 হারে ঘটে 10 এয়ার-ওয়াটার ইন্টারফেস এবং বাল্ক ওয়াটারে নয়। বরফ স্ফটিকের বৃদ্ধি বিভিন্ন বৃদ্ধির হারের উপর নির্ভর করেশক্তি জৈবিক নমুনা, খাদ্য ও অঙ্গ-প্রত্যঙ্গ সংরক্ষণ করার সময় পানিকে অবশ্যই জমাট বাঁধা থেকে রক্ষা করতে হবে।
এটি সাধারণত দ্রুত শীতল করার হার, ছোট নমুনা এবং একটি ক্রায়োকনজারভেটর ব্যবহার করে এবং নিউক্লিয়েট বরফের চাপ বৃদ্ধি করে এবং কোষের ক্ষতি রোধ করে অর্জন করা হয়। বরফ/তরলের মুক্ত শক্তি বায়ুমণ্ডলীয় চাপে ~30 mJ/m2 থেকে 40 mJ/m-2 200 MPa এ বৃদ্ধি পায়, যা নির্দেশ করে কেন এই প্রভাব দেখা দেয়।
কী ধরনের স্ফটিক জালি বরফের বৈশিষ্ট্য
বিকল্পভাবে, তারা দ্রুত হিমায়িত বা উত্তেজিত হ্রদের এলোমেলোভাবে বিঘ্নিত পৃষ্ঠে প্রিজম পৃষ্ঠ (S2) থেকে দ্রুত বৃদ্ধি পেতে পারে। {1 1 -2 0} মুখগুলি থেকে বৃদ্ধি অন্তত একই, কিন্তু তাদের প্রিজম বেসে পরিণত করে। বরফের স্ফটিক বিকাশের তথ্য সম্পূর্ণরূপে তদন্ত করা হয়েছে। বিভিন্ন মুখের উপাদানগুলির আপেক্ষিক বৃদ্ধির হার যৌথ হাইড্রেশনের বৃহৎ ডিগ্রী গঠনের ক্ষমতার উপর নির্ভর করে। আশেপাশের পানির তাপমাত্রা (নিম্ন) বরফের স্ফটিকের শাখার মাত্রা নির্ধারণ করে। কম ডিগ্রী সুপারকুলিং, অর্থাৎ <2 ডিগ্রি সেলসিয়াসে ডিফিউশন রেট দ্বারা কণার বৃদ্ধি সীমিত, যার ফলে তাদের বেশি হয়।

কিন্তু উন্নয়ন গতিবিদ্যা দ্বারা সীমিত >4 ডিগ্রি সেলসিয়াসের উচ্চ স্তরের বিষণ্নতা, যার ফলে সুচ বৃদ্ধি পায়। এই আকৃতিটি শুষ্ক বরফের কাঠামোর অনুরূপ (একটি ষড়ভুজ কাঠামো সহ একটি স্ফটিক জালি রয়েছে), বিভিন্নপৃষ্ঠের বিকাশের বৈশিষ্ট্য এবং আশেপাশের (সুপার কুলড) জলের তাপমাত্রা, যা স্নোফ্লেক্সের সমতল আকৃতির পিছনে রয়েছে।
বায়ুমন্ডলে বরফের গঠন মেঘের গঠন ও বৈশিষ্ট্যকে গভীরভাবে প্রভাবিত করে। ফেল্ডস্পার, মরুভূমির ধূলিকণাতে পাওয়া যায় যা বছরে লক্ষ লক্ষ টন বায়ুমণ্ডলে প্রবেশ করে, গুরুত্বপূর্ণ প্রাক্তন। কম্পিউটার সিমুলেশনগুলি দেখিয়েছে যে এটি উচ্চ-শক্তির পৃষ্ঠের সমতলগুলিতে প্রিজম্যাটিক বরফ স্ফটিক প্লেনের নিউক্লিয়েশনের কারণে হয়েছে৷
অন্যান্য কিছু উপাদান এবং জালি
দ্রবীভূত পদার্থগুলি (খুব ছোট হিলিয়াম এবং হাইড্রোজেন ব্যতীত, যা অন্তঃস্থলে প্রবেশ করতে পারে) বায়ুমণ্ডলীয় চাপে আইএইচ কাঠামোতে অন্তর্ভুক্ত করা যায় না, তবে কণাগুলির মধ্যে পৃষ্ঠ বা নিরাকার স্তরে জোর করে বেরিয়ে যায়। মাইক্রোক্রিস্টালাইন শরীর। শুষ্ক বরফের জালযুক্ত স্থানে আরও কিছু উপাদান রয়েছে: ক্যাওট্রপিক আয়ন যেমন NH4 + এবং Cl- যা অন্যান্য কসমোট্রপিক যেমন Na+ এবং SO42-এর তুলনায় হালকা তরল হিমায়িত করার অন্তর্ভুক্ত, তাই স্ফটিকের মধ্যে অবশিষ্ট তরলের একটি পাতলা ফিল্ম তৈরি করার কারণে তাদের অপসারণ করা সম্ভব নয়। এটি অবশিষ্ট চার্জ (যা চৌম্বকীয় বিকিরণও হতে পারে) এবং অবশিষ্ট তরল ফিল্মের pH-তে পরিবর্তন, যেমন NH 4 ভারসাম্য বজায় রাখার কারণে পৃষ্ঠের জলের বিচ্ছিন্নতার কারণে পৃষ্ঠের বৈদ্যুতিক চার্জিং হতে পারে2SO4 আরো অম্লীয় হয়ে ওঠে এবং NaCl আরও মৌলিক হয়ে ওঠে।
এগুলি মুখের সাথে লম্ববরফের স্ফটিক জালি পরবর্তী স্তর সংযুক্ত দেখাচ্ছে (কালোতে O পরমাণু সহ)। এগুলি ধীরে ধীরে ক্রমবর্ধমান বেসাল পৃষ্ঠ {0 0 0 1} দ্বারা চিহ্নিত করা হয়, যেখানে শুধুমাত্র বিচ্ছিন্ন জলের অণুগুলি সংযুক্ত থাকে। একটি প্রিজমের একটি দ্রুত বর্ধনশীল {1 0 -1 0} পৃষ্ঠ যেখানে নতুন সংযুক্ত কণার জোড়া হাইড্রোজেন (একটি হাইড্রোজেন বন্ধন/একটি মৌলের দুটি অণু) সাথে একে অপরের সাথে বন্ধন করতে পারে। দ্রুত বর্ধনশীল মুখ হল {1 1 -2 0} (সেকেন্ডারি প্রিজম্যাটিক), যেখানে নতুন সংযুক্ত কণার চেইন হাইড্রোজেন বন্ধনের মাধ্যমে একে অপরের সাথে যোগাযোগ করতে পারে। তার শৃঙ্খল/উপাদানের অণুগুলির মধ্যে একটি এমন একটি ফর্ম যা শিলাগুলি তৈরি করে যা প্রিজমের দুটি দিকে বিভক্ত করে এবং রূপান্তরকে উত্সাহিত করে৷
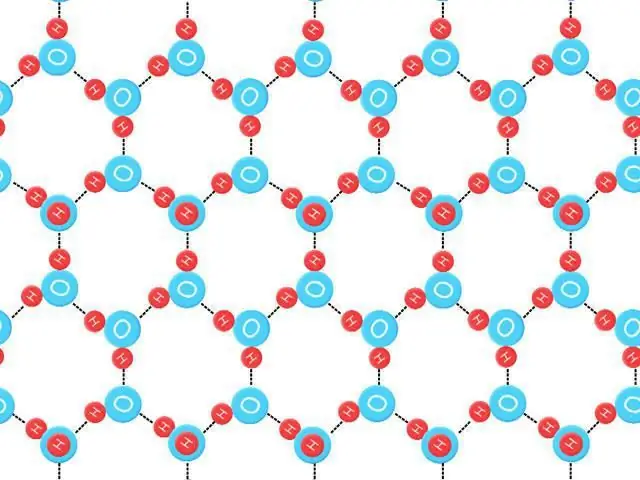
জিরো পয়েন্ট এনট্রপি
S হিসেবে সংজ্ঞায়িত করা যেতে পারে 0=k B ˣ Ln (N E0), যেখানে k B হল বোল্টজম্যান ধ্রুবক, NE হল E শক্তিতে কনফিগারেশনের সংখ্যা এবং E0 হল সর্বনিম্ন শক্তি। শূন্য কেলভিনে ষড়ভুজাকার বরফের এনট্রপির এই মান তাপগতিবিদ্যার তৃতীয় সূত্র লঙ্ঘন করে না "পরম শূন্যে একটি আদর্শ স্ফটিকের এনট্রপি ঠিক শূন্য", যেহেতু এই উপাদানগুলি এবং কণাগুলি আদর্শ নয়, হাইড্রোজেন বন্ধনকে ব্যাহত করেছে৷
এই শরীরে, হাইড্রোজেন বন্ধন এলোমেলো এবং দ্রুত পরিবর্তনশীল। এই কাঠামোগুলি শক্তিতে ঠিক সমান নয়, তবে "বরফের নিয়ম" মেনে চলা খুব বড় সংখ্যক শক্তির কাছাকাছি রাজ্যে প্রসারিত। জিরো পয়েন্ট এনট্রপি এমন একটি ব্যাধি যা উপাদানটিকে পরমভাবে ঠান্ডা করা গেলেও থাকবেশূন্য (0 K=-273, 15 ° C)। ষড়ভুজ বরফ 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1 এর জন্য পরীক্ষামূলক বিভ্রান্তি তৈরি করে। তাত্ত্বিকভাবে, এটি পরীক্ষামূলকভাবে নির্ধারণ করার চেয়ে অনেক বেশি নির্ভুলতার সাথে পরিচিত বরফের স্ফটিকগুলির শূন্য এনট্রপি গণনা করা সম্ভব হবে (ত্রুটি এবং শক্তি স্তরের বিস্তারকে উপেক্ষা করে)।
এই এলাকায় বিজ্ঞানী এবং তাদের কাজ
S হিসেবে সংজ্ঞায়িত করা যেতে পারে 0=k B ˣ Ln (N E0), যেখানে k B হল বোল্টজম্যান ধ্রুবক, NE হল E শক্তিতে কনফিগারেশনের সংখ্যা এবং E0 হল সর্বনিম্ন শক্তি। শূন্য কেলভিনে ষড়ভুজাকার বরফের এনট্রপির এই মান তাপগতিবিদ্যার তৃতীয় সূত্র লঙ্ঘন করে না "পরম শূন্যে একটি আদর্শ স্ফটিকের এনট্রপি ঠিক শূন্য", যেহেতু এই উপাদানগুলি এবং কণাগুলি আদর্শ নয়, হাইড্রোজেন বন্ধনকে ব্যাহত করেছে৷
এই শরীরে, হাইড্রোজেন বন্ধন এলোমেলো এবং দ্রুত পরিবর্তনশীল। এই কাঠামোগুলি শক্তিতে ঠিক সমান নয়, তবে "বরফের নিয়ম" মেনে চলা খুব বড় সংখ্যক শক্তির কাছাকাছি রাজ্যে প্রসারিত। জিরো পয়েন্ট এনট্রপি এমন একটি ব্যাধি যা উপাদানটিকে নিখুঁত শূন্য (0 K=-273.15°C) এ ঠান্ডা করা গেলেও থাকবে। ষড়ভুজ বরফ 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1 এর জন্য পরীক্ষামূলক বিভ্রান্তি তৈরি করে। তাত্ত্বিকভাবে, এটি পরীক্ষামূলকভাবে নির্ধারণ করার চেয়ে অনেক বেশি নির্ভুলতার সাথে পরিচিত বরফের স্ফটিকগুলির শূন্য এনট্রপি গণনা করা সম্ভব হবে (ত্রুটি এবং শক্তি স্তরের বিস্তারকে উপেক্ষা করে)।

যদিও বাল্ক বরফে প্রোটনের ক্রম নির্ধারণ করা হয় না, তবে পৃষ্ঠ সম্ভবত ঝুলন্ত এইচ-পরমাণু এবং ও-একক জোড়ার ব্যান্ডের আকারে এই কণাগুলির ক্রম পছন্দ করে (অর্ডারযুক্ত হাইড্রোজেন বন্ড সহ শূন্য এনট্রপি)। জিরো পয়েন্ট ডিসঅর্ডার ZPE, J ˣ mol -1 ˣ K -1 এবং অন্যান্য পাওয়া যায়। উপরের সবগুলো থেকে, এটা পরিষ্কার এবং বোধগম্য যে কি ধরনের স্ফটিক জালি বরফের বৈশিষ্ট্য।






