একটি গ্যাসের তাপ ক্ষমতা হ'ল একটি ডিগ্রী উত্তপ্ত হলে একটি শরীর যে পরিমাণ শক্তি শোষণ করে। আসুন এই শারীরিক পরিমাণের প্রধান বৈশিষ্ট্যগুলি বিশ্লেষণ করি৷

সংজ্ঞা
একটি গ্যাসের নির্দিষ্ট তাপ হল একটি নির্দিষ্ট পদার্থের একক ভর। এর পরিমাপের একক হল J/(kg·K)। একত্রিতকরণের অবস্থার পরিবর্তনের প্রক্রিয়ায় শরীর দ্বারা যে পরিমাণ তাপ শোষিত হয় তা শুধুমাত্র প্রাথমিক এবং চূড়ান্ত অবস্থার সাথেই নয়, পরিবর্তনের পদ্ধতির সাথেও জড়িত।

বিভাগ
গ্যাসের তাপ ক্ষমতা ধ্রুবক আয়তনে নির্ধারিত মান দ্বারা ভাগ করা হয় (Cv), ধ্রুব চাপ (Cр)।
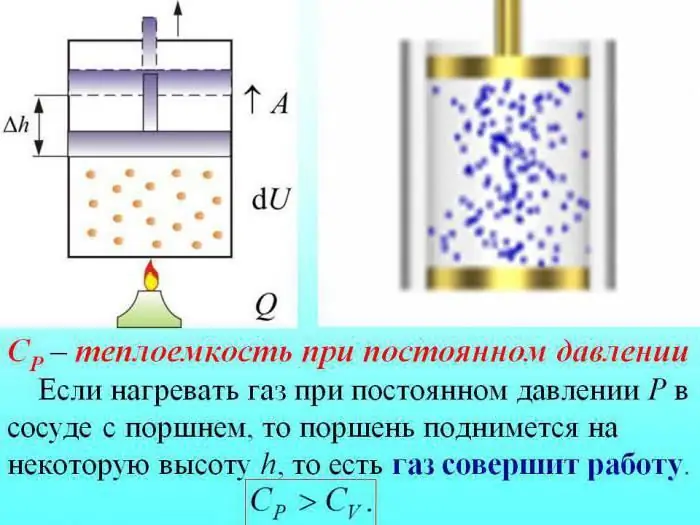
চাপের পরিবর্তন না করে গরম করার ক্ষেত্রে, গ্যাস সম্প্রসারণের কাজে কিছু তাপ ব্যয় করা হয় এবং শক্তির কিছু অংশ অভ্যন্তরীণ শক্তি বৃদ্ধিতে ব্যয় করা হয়।
ধ্রুব চাপে গ্যাসের তাপ ক্ষমতা অভ্যন্তরীণ শক্তি বৃদ্ধিতে ব্যয় করা তাপের পরিমাণ দ্বারা নির্ধারিত হয়।
গ্যাসের অবস্থা: বৈশিষ্ট্য, বিবরণ
একটি আদর্শ গ্যাসের তাপ ক্ষমতা নির্ধারণ করা হয় এই বিষয়টি বিবেচনায় নিয়ে যে Сp-Сv=R। শেষের পরিমাণকে সর্বজনীন গ্যাস ধ্রুবক বলা হয়। এর মান 8.314 J/(mol K) এর সাথে মিলে যায়।
তাপ ক্ষমতার তাত্ত্বিক গণনা করার সময়, উদাহরণস্বরূপ, তাপমাত্রার সাথে সম্পর্ক বর্ণনা করার সময়, শুধুমাত্র থার্মোডাইনামিক পদ্ধতি ব্যবহার করাই যথেষ্ট নয়, স্থির পদার্থবিদ্যার উপাদানগুলির সাথে নিজেকে সজ্জিত করা গুরুত্বপূর্ণ৷
গ্যাসের তাপ ক্ষমতার মধ্যে কিছু অণুর অনুবাদমূলক গতির শক্তির গড় মানের গণনা জড়িত। এই ধরনের আন্দোলন অণুর ঘূর্ণন এবং অনুবাদমূলক গতির পাশাপাশি পরমাণুর অভ্যন্তরীণ কম্পন থেকে সংক্ষিপ্ত করা হয়।
স্থির পদার্থবিজ্ঞানে, এমন তথ্য রয়েছে যে ঘূর্ণনগত এবং অনুবাদমূলক গতির স্বাধীনতার প্রতিটি ডিগ্রির জন্য, একটি গ্যাসের জন্য একটি পরিমাণ রয়েছে যা সর্বজনীন গ্যাস ধ্রুবকের অর্ধেক সমান।

আকর্ষণীয় তথ্য
একটি মোনাটমিক গ্যাসের একটি কণার স্বাধীনতার তিনটি অনুবাদমূলক ডিগ্রী রয়েছে বলে ধরে নেওয়া হয়, তাই একটি গ্যাসের নির্দিষ্ট তাপের তিনটি অনুবাদমূলক, দুটি ঘূর্ণনশীল এবং একটি কম্পন ডিগ্রী স্বাধীনতা রয়েছে। তাদের অভিন্ন বণ্টনের নিয়মটি নির্দিষ্ট তাপকে ধ্রুবক আয়তনে R.
এ সমান করে দেয়
পরীক্ষা চলাকালীন, এটি পাওয়া গেছে যে একটি ডায়াটমিক গ্যাসের তাপ ক্ষমতা R-এর মানের সাথে মিলে যায়। তত্ত্ব এবং অনুশীলনের মধ্যে এই ধরনের বৈষম্যটি এই সত্য দ্বারা ব্যাখ্যা করা হয়েছে যে একটি আদর্শ গ্যাসের তাপ ক্ষমতা কোয়ান্টামের সাথে যুক্ত। প্রভাব, অতএব, গণনা করার সময়, কোয়ান্টামের উপর ভিত্তি করে পরিসংখ্যান ব্যবহার করা গুরুত্বপূর্ণমেকানিক্স।
কোয়ান্টাম মেকানিক্সের ভিত্তির উপর ভিত্তি করে, গ্যাসের অণু সহ দোদুল্যমান বা ঘোরানো কণার যে কোনও সিস্টেমে শক্তির কিছু বিচ্ছিন্ন মান রয়েছে।
যদি সিস্টেমে তাপীয় গতির শক্তি একটি নির্দিষ্ট কম্পাঙ্কের দোলনকে উত্তেজিত করার জন্য যথেষ্ট না হয় তবে এই ধরনের গতিগুলি সিস্টেমের মোট তাপ ক্ষমতায় অবদান রাখে না।
ফলস্বরূপ, স্বাধীনতার একটি নির্দিষ্ট মাত্রা "হিমায়িত" হয়ে যায়, এটিতে সম-বিভাগের আইন প্রয়োগ করা অসম্ভব৷
গ্যাসের তাপ ক্ষমতা রাষ্ট্রের একটি গুরুত্বপূর্ণ বৈশিষ্ট্য যার উপর সমগ্র থার্মোডাইনামিক সিস্টেমের কার্যকারিতা নির্ভর করে।
যে তাপমাত্রায় সমবিভাজন আইনটি স্বাধীনতার কম্পন বা ঘূর্ণনগত ডিগ্রিতে প্রয়োগ করা যেতে পারে তা কোয়ান্টাম তত্ত্ব দ্বারা চিহ্নিত করা হয়, যা প্ল্যাঙ্ক ধ্রুবককে বোল্টজম্যান ধ্রুবকের সাথে সংযুক্ত করে।

ডায়াটমিক গ্যাস
এই জাতীয় গ্যাসগুলির ঘূর্ণন শক্তির স্তরগুলির মধ্যে ব্যবধানগুলি অল্প সংখ্যক ডিগ্রি। ব্যতিক্রম হল হাইড্রোজেন, যেখানে তাপমাত্রার মান শত শত ডিগ্রী দ্বারা নির্ধারিত হয়।
এই কারণেই ধ্রুবক চাপে গ্যাসের তাপ ক্ষমতা অভিন্ন বন্টনের আইন দ্বারা বর্ণনা করা কঠিন। কোয়ান্টাম পরিসংখ্যানে, তাপের ক্ষমতা নির্ধারণ করার সময়, এটি বিবেচনায় নেওয়া হয় যে তাপমাত্রা হ্রাসের ক্ষেত্রে এর কম্পনের অংশটি দ্রুত হ্রাস পায় এবং শূন্যে পৌঁছে যায়।
এই ঘটনাটি ব্যাখ্যা করে যে ঘরের তাপমাত্রায় কার্যত তাপ ক্ষমতার কোন কম্পনশীল অংশ নেইডায়াটমিক গ্যাস, এটি ধ্রুবক R.
এর সাথে মিলে যায়
নিম্ন তাপমাত্রা সূচকের ক্ষেত্রে ধ্রুবক আয়তনে গ্যাসের তাপ ক্ষমতা কোয়ান্টাম পরিসংখ্যান ব্যবহার করে নির্ধারিত হয়। Nernst নীতি আছে, যাকে তাপগতিবিদ্যার তৃতীয় সূত্র বলা হয়। এর গঠনের উপর ভিত্তি করে, একটি গ্যাসের মোলার তাপ ক্ষমতা হ্রাসের তাপমাত্রার সাথে হ্রাস পাবে, শূন্যের দিকে ঝুঁকবে।

কঠিন পদার্থের বৈশিষ্ট্য
যদি কোয়ান্টাম পরিসংখ্যান ব্যবহার করে গ্যাসের মিশ্রণের তাপ ক্ষমতা ব্যাখ্যা করা যায়, তাহলে একত্রিতকরণের কঠিন অবস্থার জন্য, তাপীয় গতি ভারসাম্য অবস্থানের কাছাকাছি কণার সামান্য ওঠানামা দ্বারা চিহ্নিত করা হয়।
প্রতিটি পরমাণুর স্বাধীনতার তিনটি কম্পনশীল ডিগ্রী রয়েছে, তাই, সমতা বিধান অনুসারে, একটি কঠিনের মোলার তাপ ক্ষমতা 3nR হিসাবে গণনা করা যেতে পারে, n একটি অণুর পরমাণুর সংখ্যা।
অভ্যাসে, এই সংখ্যাটি এমন একটি সীমা যা একটি কঠিন শরীরের তাপ ক্ষমতা উচ্চ তাপমাত্রায় থাকে।
ধাতু সহ কিছু উপাদানের জন্য সাধারণ তাপমাত্রায় সর্বাধিক প্রাপ্ত করা যেতে পারে। n=1 এর জন্য, Dulong এবং Petit আইন পূর্ণ, কিন্তু জটিল পদার্থের জন্য এই ধরনের সীমাতে পৌঁছানো বেশ কঠিন। যেহেতু সীমা বাস্তবে পাওয়া যায় না, তাই কঠিন পদার্থের পচন বা গলে যায়।
কোয়ান্টাম তত্ত্বের ইতিহাস
কোয়ান্টাম তত্ত্বের প্রতিষ্ঠাতা হলেন বিংশ শতাব্দীর শুরুতে আইনস্টাইন এবং ডেবাই। এটি একটি নির্দিষ্ট পরমাণুর দোলক গতির পরিমাণ নির্ধারণের উপর ভিত্তি করেস্ফটিক নিম্ন তাপমাত্রা সূচকের ক্ষেত্রে, একটি কঠিন শরীরের তাপ ক্ষমতা ঘনক্ষেত্রে নেওয়া পরম মানের সাথে সরাসরি সমানুপাতিক হতে দেখা যায়। এই সম্পর্ককে ডেবাইয়ের আইন বলা হয়েছে। নিম্ন এবং উচ্চ তাপমাত্রার সূচকগুলির মধ্যে পার্থক্য করা সম্ভব করে এমন একটি মানদণ্ড হিসাবে, Debye তাপমাত্রার সাথে তাদের তুলনা করা হয়৷
এই মানটি শরীরের একটি পরমাণুর কম্পনের বর্ণালী দ্বারা নির্ধারিত হয়, তাই এটি গুরুতরভাবে এর স্ফটিক কাঠামোর বৈশিষ্ট্যগুলির উপর নির্ভর করে।
QD হল এমন একটি মান যার কয়েকশ K আছে, কিন্তু, উদাহরণস্বরূপ, এটি হীরাতে অনেক বেশি।
পরিবাহী ইলেকট্রন ধাতুর তাপ ক্ষমতায় গুরুত্বপূর্ণ অবদান রাখে। এটি গণনা করতে, ফার্মি কোয়ান্টাম পরিসংখ্যান ব্যবহার করা হয়। ধাতব পরমাণুর ইলেকট্রনিক পরিবাহিতা পরম তাপমাত্রার সরাসরি সমানুপাতিক। যেহেতু এটি একটি নগণ্য মান, এটি শুধুমাত্র পরম শূন্যের প্রবণতা তাপমাত্রায় বিবেচনা করা হয়।
তাপ ক্ষমতা নির্ধারণের পদ্ধতি
প্রধান পরীক্ষামূলক পদ্ধতি হল ক্যালোরিমেট্রি। তাপ ক্ষমতার একটি তাত্ত্বিক গণনা করতে, পরিসংখ্যানগত তাপগতিবিদ্যা ব্যবহার করা হয়। এটি একটি আদর্শ গ্যাসের জন্য বৈধ, সেইসাথে স্ফটিক দেহগুলির জন্য, পদার্থের কাঠামোর উপর পরীক্ষামূলক তথ্যের ভিত্তিতে সঞ্চালিত হয়৷
একটি আদর্শ গ্যাসের তাপ ক্ষমতা গণনার জন্য পরীক্ষামূলক পদ্ধতিগুলি রাসায়নিক কাঠামোর ধারণার উপর ভিত্তি করে তৈরি করা হয়, Ср এ পরমাণুর পৃথক গোষ্ঠীর অবদান।
তরলগুলির জন্য, পদ্ধতিগুলিও ব্যবহার করা হয় যা থার্মোডাইনামিক ব্যবহারের উপর ভিত্তি করেচক্র যা বাষ্পীভবন প্রক্রিয়ার এনথালপির তাপমাত্রার ডেরিভেটিভের মাধ্যমে একটি আদর্শ গ্যাসের তাপ ক্ষমতা থেকে একটি তরলে স্থানান্তর করা সম্ভব করে৷
একটি সমাধানের ক্ষেত্রে, একটি সংযোজন ফাংশন হিসাবে তাপ ক্ষমতার গণনা অনুমোদিত নয়, যেহেতু দ্রবণের তাপ ক্ষমতার অতিরিক্ত মান মূলত তাৎপর্যপূর্ণ।
এটি মূল্যায়ন করতে, আমাদের সমাধানের আণবিক-পরিসংখ্যান তত্ত্ব প্রয়োজন। থার্মোডাইনামিক বিশ্লেষণে ভিন্নধর্মী সিস্টেমের তাপ ক্ষমতা সনাক্ত করা সবচেয়ে কঠিন।

উপসংহার
তাপ ক্ষমতার অধ্যয়ন আপনাকে রাসায়নিক চুল্লিতে, সেইসাথে অন্যান্য রাসায়নিক উত্পাদন যন্ত্রপাতিগুলিতে ঘটে যাওয়া প্রক্রিয়াগুলির শক্তির ভারসাম্য গণনা করতে দেয়। এছাড়াও, সর্বোত্তম ধরণের কুল্যান্ট নির্বাচনের জন্য এই মানটি প্রয়োজনীয়৷
বর্তমানে, বিভিন্ন তাপমাত্রার ব্যবধানের জন্য পদার্থের তাপ ক্ষমতার পরীক্ষামূলক নির্ণয় - নিম্ন মান থেকে উচ্চ মান পর্যন্ত - একটি পদার্থের তাপগতিগত বৈশিষ্ট্য নির্ধারণের প্রধান বিকল্প। একটি পদার্থের এনট্রপি এবং এনথালপি গণনা করার সময়, তাপ ক্ষমতা অখণ্ড ব্যবহার করা হয়। একটি নির্দিষ্ট তাপমাত্রা পরিসরে রাসায়নিক বিকারকগুলির তাপ ক্ষমতা সম্পর্কে তথ্য আপনাকে প্রক্রিয়াটির তাপীয় প্রভাব গণনা করতে দেয়। সমাধানগুলির তাপ ক্ষমতা সম্পর্কিত তথ্য বিশ্লেষণকৃত ব্যবধানের মধ্যে যে কোনও তাপমাত্রার মানগুলিতে তাদের তাপগতিগত পরামিতিগুলি গণনা করা সম্ভব করে তোলে৷
উদাহরণস্বরূপ, একটি তরল সম্ভাব্য শক্তির মান পরিবর্তন করতে তাপের কিছু অংশ ব্যয় দ্বারা চিহ্নিত করা হয়প্রতিক্রিয়াশীল অণু। এই মানটিকে "কনফিগারেশন" তাপ ক্ষমতা বলা হয়, যা সমাধানগুলি বর্ণনা করতে ব্যবহৃত হয়৷
একটি পদার্থের থার্মোডাইনামিক বৈশিষ্ট্য, এর সমষ্টির অবস্থা বিবেচনা না করে পূর্ণাঙ্গ গাণিতিক গণনা পরিচালনা করা কঠিন। এই কারণেই তরল, গ্যাস, কঠিন পদার্থের জন্য নির্দিষ্ট তাপ ক্ষমতার মতো একটি বৈশিষ্ট্য ব্যবহার করা হয়, যা একটি পদার্থের শক্তির পরামিতিগুলিকে চিহ্নিত করা সম্ভব করে।






