আমাদের সময়ে, পদার্থবিদ্যা একটি অতি সাধারণ বিজ্ঞানে পরিণত হয়েছে। এটি আক্ষরিকভাবে সর্বত্র উপস্থিত। সবচেয়ে প্রাথমিক উদাহরণ: আপনার উঠোনে একটি আপেল গাছ বেড়ে ওঠে এবং তাতে ফল পাকে, সময় আসে এবং আপেল পড়তে শুরু করে, কিন্তু তারা কোন দিকে পড়ে? সার্বজনীন মাধ্যাকর্ষণ আইনের জন্য ধন্যবাদ, আমাদের ভ্রূণ মাটিতে পড়ে, অর্থাৎ, এটি নীচে যায়, কিন্তু উপরে নয়। এটি পদার্থবিদ্যার সবচেয়ে বিখ্যাত উদাহরণগুলির মধ্যে একটি ছিল, তবে আসুন তাপগতিবিদ্যার দিকে মনোযোগ দেই, বা আরও স্পষ্টভাবে, ফেজ ভারসাম্যের দিকে, যা আমাদের জীবনে কম গুরুত্বপূর্ণ নয়৷
তাপগতিবিদ্যা

প্রথমত, আসুন এই শব্দটি দেখি। ΘερΜοδυναΜική - এই শব্দটি গ্রীক ভাষায় দেখায়। প্রথম অংশ ΘερΜo অর্থ "উষ্ণতা" এবং দ্বিতীয় অংশের অর্থ "শক্তি"। তাপগতিবিদ্যা হল পদার্থবিজ্ঞানের একটি শাখা যা একটি ম্যাক্রোস্কোপিক সিস্টেমের বৈশিষ্ট্যগুলি, সেইসাথে শক্তি রূপান্তর এবং স্থানান্তর করার বিভিন্ন উপায়গুলি অধ্যয়ন করে। এই বিভাগে, বিভিন্ন অবস্থা এবং প্রক্রিয়াগুলি বিশেষভাবে অধ্যয়ন করা হয় যাতে তাপমাত্রার ধারণাটি বর্ণনায় প্রবর্তন করা যায় (এটি একটি ভৌত পরিমাণ যা একটি থার্মোডাইনামিক সিস্টেমকে চিহ্নিত করে এবং এটি ব্যবহার করে পরিমাপ করা হয়নির্দিষ্ট যন্ত্রপাতি)। থার্মোডাইনামিক সিস্টেমে চলমান সমস্ত প্রক্রিয়া শুধুমাত্র মাইক্রোস্কোপিক পরিমাণ (চাপ এবং তাপমাত্রা, সেইসাথে উপাদানগুলির ঘনত্ব) দ্বারা বর্ণিত হয়।
ক্লেপিরন-ক্লসিয়াস সমীকরণ
প্রতিটি পদার্থবিজ্ঞানী এই সমীকরণটি জানেন, তবে আসুন এটিকে টুকরো টুকরো করে ভেঙে ফেলা যাক। এটি নির্দিষ্ট পদার্থের এক পর্যায় থেকে অন্য পর্যায়ে স্থানান্তরের ভারসাম্য প্রক্রিয়াকে বোঝায়। এই ধরনের উদাহরণগুলিতে এটি স্পষ্টভাবে দেখা যায়: গলে যাওয়া, বাষ্পীভবন, পরমানন্দ (পণ্য সংরক্ষণের একটি উপায়, যা সম্পূর্ণরূপে আর্দ্রতা অপসারণ করে)। সূত্রটি স্পষ্টভাবে চলমান প্রক্রিয়াগুলি দেখায়:
- n=PV/RT;
- যেখানে T হল পদার্থের তাপমাত্রা;
- P-চাপ;
- R-নির্দিষ্ট তাপ পর্যায় পরিবর্তনের;
- V- নির্দিষ্ট ভলিউমে পরিবর্তন।
সমীকরণ তৈরির ইতিহাস

ক্লাসিয়াস-ক্ল্যাপেয়ারন সমীকরণটি তাপগতিবিদ্যার দ্বিতীয় সূত্রের একটি চমৎকার গাণিতিক ব্যাখ্যা। এছাড়াও "ক্লসিয়াস অসমতা" হিসাবে উল্লেখ করা হয়। স্বাভাবিকভাবেই, তত্ত্বটি বিজ্ঞানী নিজেই তৈরি করেছিলেন, যিনি সিস্টেমে তাপ প্রবাহ এবং এনট্রপির পাশাপাশি এর পরিবেশের মধ্যে সম্পর্ক ব্যাখ্যা করতে চেয়েছিলেন। এই সমীকরণটি ক্লসিয়াস দ্বারা এনট্রপি ব্যাখ্যা এবং পরিমাপ করার প্রচেষ্টায় তৈরি করা হয়েছিল। আক্ষরিক অর্থে, তত্ত্বটি আমাদের নির্ধারণ করার সুযোগ দেয় যে একটি চক্রীয় প্রক্রিয়া বিপরীত বা অপরিবর্তনীয় কিনা। এই অসমতা আমাদের দ্বিতীয় আইন বোঝার জন্য একটি পরিমাণগত সূত্র প্রদান করে৷
এই বিজ্ঞানী ছিলেন এনট্রপির ধারণা নিয়ে কাজ করা প্রথম ব্যক্তিদের একজন, এমনকি এটি দিয়েছিলেনপ্রক্রিয়ার নাম. যেটি এখন ক্লসিয়াসের উপপাদ্য নামে পরিচিত তা 1862 সালে রুডলফের ষষ্ঠ রচনা, অভ্যন্তরীণ কাজের জন্য রূপান্তর সমতুল্য তত্ত্বের ব্যবহারে প্রথম প্রকাশিত হয়েছিল। বিজ্ঞানী সিস্টেমে গরম (δ Q) দ্বারা এনট্রপি এবং শক্তি প্রবাহের মধ্যে একটি আনুপাতিক সম্পর্ক দেখানোর চেষ্টা করেছিলেন। নির্মাণে, এই তাপ শক্তিকে কাজে রূপান্তরিত করা যেতে পারে, এবং এটি একটি চক্রীয় প্রক্রিয়ার মাধ্যমে তাপে রূপান্তরিত হতে পারে। রুডলফ প্রমাণ করেছিলেন যে "চক্রীয় প্রক্রিয়ায় ঘটে যাওয়া সমস্ত রূপান্তরের বীজগাণিতিক যোগফল শুধুমাত্র শূন্যের কম হতে পারে বা চরম ক্ষেত্রে শূন্যের সমান হতে পারে।"
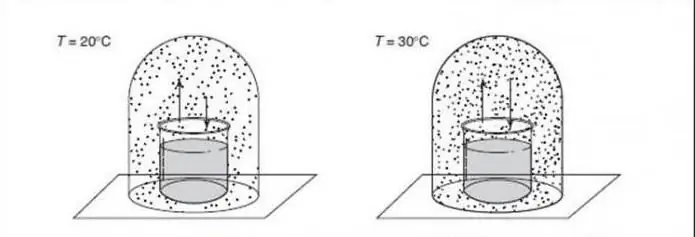
বন্ধ বিচ্ছিন্ন সিস্টেম
বিচ্ছিন্ন সিস্টেম নিম্নলিখিতগুলির মধ্যে একটি:
- শারীরিক ব্যবস্থা অন্যদের থেকে দূরে যা তাদের সাথে যোগাযোগ করে না।
- থার্মোডাইনামিক সিস্টেমটি অনমনীয় স্থাবর দেয়াল দ্বারা বন্ধ থাকে যার মধ্য দিয়ে পদার্থ বা শক্তি কোনটাই যেতে পারে না।
অভ্যন্তরীণভাবে বিষয়টি তার নিজস্ব মাধ্যাকর্ষণ এর সাথে সম্পর্কিত হওয়া সত্ত্বেও, একটি বিচ্ছিন্ন সিস্টেমকে সাধারণত বাহ্যিক মহাকর্ষীয় এবং অন্যান্য দূরবর্তী শক্তির সীমা অতিক্রম করা হয়।
এর সাথে বৈপরীত্য হতে পারে (তাপগতিবিদ্যায় ব্যবহৃত আরও সাধারণ পরিভাষায়) নির্বাচনী দেয়াল দ্বারা বেষ্টিত একটি বদ্ধ ব্যবস্থা বলা হয় যার মাধ্যমে তাপ বা কাজের আকারে শক্তি স্থানান্তর করা যেতে পারে, কিন্তু ব্যাপার নয়। এবং একটি উন্মুক্ত ব্যবস্থার সাথে যেখানে পদার্থ এবং শক্তি প্রবেশ করে বা প্রস্থান করে, যদিও এতে বিভিন্ন দুর্ভেদ্য দেয়াল থাকতে পারে।এর সীমানার কিছু অংশ।
একটি বিচ্ছিন্ন ব্যবস্থা সংরক্ষণ আইন মেনে চলে। প্রায়শই তাপগতিবিদ্যায় পদার্থ এবং শক্তিকে পৃথক ধারণা হিসাবে বিবেচনা করা হয়।
থার্মোডাইনামিক ট্রানজিশন
কোয়ান্টাম ফেজ ট্রানজিশন বোঝার জন্য, তাদের ক্লাসিক্যাল ট্রান্সফরমেশনের সাথে তুলনা করা উপকারী (এটিকে তাপীয় ইনভার্সনও বলা হয়)। CPT একটি সিস্টেমের থার্মোডাইনামিক বৈশিষ্ট্যের মধ্যে cusp বর্ণনা করে। এটি কণার পুনর্গঠনের সংকেত দেয়। একটি সাধারণ উদাহরণ হল জলের হিমায়িত রূপান্তর, যা একটি তরল এবং একটি কঠিনের মধ্যে একটি মসৃণ রূপান্তর বর্ণনা করে। ক্লাসিক্যাল ফেজ বৃদ্ধি সিস্টেমের শক্তি এবং এর তাপীয় ওঠানামার এনট্রপির মধ্যে প্রতিযোগিতার কারণে হয়।
একটি ধ্রুপদী সিস্টেমের শূন্য তাপমাত্রায় কোন এনট্রপি নেই এবং তাই কোন পর্যায়ের রূপান্তর ঘটতে পারে না। তাদের ক্রম প্রথম বিচ্ছিন্ন ডেরিভেটিভ থার্মোডাইনামিক সম্ভাব্য দ্বারা নির্ধারিত হয়। এবং, অবশ্যই, এটি প্রথম আদেশ আছে. একটি ফেরোম্যাগনেট থেকে প্যারাম্যাগনেটে পর্যায় রূপান্তরগুলি অবিচ্ছিন্ন এবং দ্বিতীয় ক্রম। একটি আদেশকৃত থেকে একটি বিশৃঙ্খল পর্যায়ে এই ধ্রুবক পরিবর্তনগুলি একটি অর্ডার প্যারামিটার দ্বারা বর্ণনা করা হয় যা শূন্য। উপরের ফেরোম্যাগনেটিক ট্রান্সফর্মেশনের জন্য, অর্ডার প্যারামিটার হবে সিস্টেমের মোট চুম্বককরণ।
গিবস সম্ভাব্য
গিবস ফ্রি এনার্জি হল প্রসারণ ছাড়াই সর্বাধিক পরিমাণ কাজ যা একটি থার্মোডাইনামিক ক্লোজড সিস্টেম থেকে সরানো যেতে পারে (যা তাপ বিনিময় করতে পারে এবং পরিবেশের সাথে কাজ করতে পারে)। যেমনসর্বাধিক ফলাফল শুধুমাত্র একটি সম্পূর্ণ বিপরীত প্রক্রিয়ায় প্রাপ্ত করা যেতে পারে। যখন সিস্টেমটি প্রথম অবস্থা থেকে দ্বিতীয় অবস্থায় রূপান্তরিত হয়, তখন গিবস মুক্ত শক্তির হ্রাস তার পরিবেশে সিস্টেম দ্বারা সম্পাদিত শক্তির সমান হয়, চাপ শক্তির কাজকে বিয়োগ করে।
ব্যালেন্সের অবস্থা

থার্মোডাইনামিক এবং যান্ত্রিক ভারসাম্য তাপগতিবিদ্যার একটি স্বতঃসিদ্ধ ধারণা। এটি এক বা একাধিক সিস্টেমের অভ্যন্তরীণ অবস্থা যা কম-বেশি প্রবেশযোগ্য বা অভেদ্য দেয়াল দ্বারা সংযুক্ত। এই অবস্থায়, কোনো সিস্টেমের মধ্যে বা সিস্টেমের মধ্যে পদার্থ বা শক্তির কোনো বিশুদ্ধ ম্যাক্রোস্কোপিক প্রবাহ নেই।
অভ্যন্তরীণ ভারসাম্যের অবস্থার নিজস্ব ধারণায়, ম্যাক্রোস্কোপিক পরিবর্তন ঘটে না। সিস্টেমগুলি একই সাথে পারস্পরিক তাপীয়, যান্ত্রিক, রাসায়নিক (ধ্রুবক), বিকিরণ ভারসাম্যের মধ্যে রয়েছে। তারা একই ফর্ম হতে পারে. এই প্রক্রিয়ায়, সমস্ত দৃশ্য একবারে এবং অনির্দিষ্টকালের জন্য সংরক্ষিত হয় যতক্ষণ না শারীরিক অপারেশনটি ভেঙে যায়। ম্যাক্রোস্কোপিক ভারসাম্যের মধ্যে, পুরোপুরি সুনির্দিষ্ট সুষম বিনিময় সঞ্চালিত হয়। উপরের প্রমাণটি এই ধারণাটির একটি শারীরিক ব্যাখ্যা৷
বেসিক
প্রতিটি আইন, উপপাদ্য, সূত্রের নিজস্ব ভিত্তি আছে। আসুন ফেজ ভারসাম্যের আইনের 3 টি ভিত্তি দেখি।
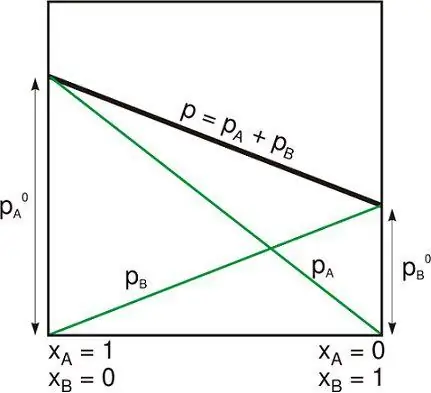
- ফেজ হল পদার্থের একটি রূপ, রাসায়নিক গঠন, ভৌত অবস্থা এবং যান্ত্রিক ভারসাম্যে একজাত। সাধারণ পর্যায়গুলি কঠিন, তরল এবং বায়বীয়।একটি পৃথক সীমানা দ্বারা বিভক্ত দুটি অবিচ্ছিন্ন তরল (বা বিভিন্ন রচনা সহ তরল মিশ্রণ) দুটি স্বতন্ত্র পর্যায় এবং অপরিবর্তনীয় কঠিন পদার্থ হিসাবে বিবেচিত হয়৷
- উপাদানের সংখ্যা (C) হল সিস্টেমের রাসায়নিকভাবে স্বাধীন উপাদানের সংখ্যা। সিস্টেমের সমস্ত পর্যায়ের গঠন নির্ধারণের জন্য প্রয়োজনীয় স্বাধীন প্রজাতির ন্যূনতম সংখ্যা।
- এই প্রসঙ্গে স্বাধীনতার ডিগ্রির সংখ্যা (F) হল নিবিড় ভেরিয়েবলের সংখ্যা যা একে অপরের থেকে স্বাধীন।
ফেজ ভারসাম্য অনুসারে শ্রেণীবিভাগ
- বিভিন্ন কম্পোজিশনের কঠিন পদার্থের মধ্যে ক্রমাগত নেট স্থানান্তরের প্রতিক্রিয়া (প্রায়ই কঠিন অবস্থার প্রতিক্রিয়া বলা হয়) ঘটে। তারা তরল পদার্থে (H, C) প্রাপ্ত উপাদানগুলিকে অন্তর্ভুক্ত করতে পারে, কিন্তু এই উপাদানগুলি কঠিন পর্যায়গুলিতে ধরে রাখা হয়, তাই কোন তরল পর্যায়গুলি বিক্রিয়ক বা পণ্য হিসাবে জড়িত নয় (H2O, CO2)। কঠিন বিশুদ্ধ স্থানান্তর প্রতিক্রিয়া ক্রমাগত বা বিরতিহীন, বা টার্মিনাল হতে পারে।
- পলিমরফিক হল এক বিশেষ ধরনের কঠিন পর্যায় বিক্রিয়া যা অভিন্ন রচনার পর্যায়গুলি অন্তর্ভুক্ত করে। শাস্ত্রীয় উদাহরণ হল অ্যালুমিনিয়াম সিলিকেট কায়ানাইট-সিলিমানাইট-অ্যান্ডালুসাইটের মধ্যে বিক্রিয়া, উচ্চ চাপে গ্রাফাইটের হীরাতে রূপান্তর এবং ক্যালসিয়াম কার্বনেটের ভারসাম্য।
ভারসাম্যের আইন

গিবস ফ্যাক্টরি রুলটি জোসিয়া উইলার্ড গিবস তার বিখ্যাত গবেষণাপত্র "দ্য ইকুইলিব্রিয়াম অফ হেটেরোজিনাস সাবস্টেন্স"-এ প্রস্তাব করেছিলেন, যা 1875 থেকে 1878 পর্যন্ত প্রকাশিত হয়েছিল। এটা প্রযোজ্যথার্মোডাইনামিক ভারসাম্যে অ-প্রতিক্রিয়াশীল বহু উপাদান ভিন্নধর্মী সিস্টেম এবং একটি প্রদত্ত সমতা:
- F=C-P+2;
- যেখানে F স্বাধীনতার ডিগ্রির সংখ্যা;
- C - উপাদানের সংখ্যা;
- P - একে অপরের সাথে থার্মোডাইনামিক ভারসাম্যের পর্যায়ের সংখ্যা।
স্বাধীনতার ডিগ্রীর সংখ্যা হল অব্যক্ত নিবিড় ভেরিয়েবলের সংখ্যা। তাপমাত্রা বা চাপের মতো থার্মোডাইনামিক পরামিতিগুলির বৃহত্তম সংখ্যা, যা একে অপরকে প্রভাবিত না করেই একযোগে এবং নির্বিচারে পরিবর্তিত হতে পারে। এক-উপাদান ব্যবস্থার উদাহরণ হল একটি একক বিশুদ্ধ রাসায়নিক সহ, যখন দুই-উপাদান ব্যবস্থা, যেমন জল এবং ইথানলের মিশ্রণে দুটি স্বাধীন উপাদান থাকে। সাধারণ ফেজ ট্রানজিশন (ফেজ ভারসাম্য) হল কঠিন, তরল, গ্যাস।
ধ্রুব চাপে ধাপের নিয়ম
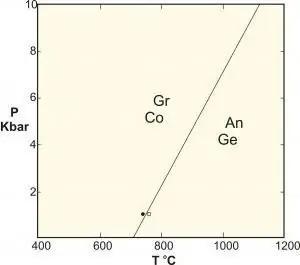
বিভিন্ন কঠিন কাঠামোর মধ্যে পর্যায় পরিবর্তনের সাথে সম্পর্কিত পদার্থ বিজ্ঞানের অ্যাপ্লিকেশনগুলির জন্য, একটি ধ্রুবক চাপ প্রায়শই ঘটে (যেমন একটি বায়ুমণ্ডল) এবং স্বাধীনতার ডিগ্রি হিসাবে উপেক্ষা করা হয়, তাই নিয়মটি হয়ে যায়: F=C - P + 1.
এই সূত্রটি কখনও কখনও "কনডেন্সড ফেজ রুল" নামে প্রবর্তিত হয়, কিন্তু আমরা জানি, এটি এই সিস্টেমগুলির ক্ষেত্রে প্রযোজ্য নয় যেগুলি উচ্চ চাপের (উদাহরণস্বরূপ, ভূতত্ত্বে), কারণ এইগুলির ফলাফলগুলি চাপের কারণে বিপর্যয়কর পরিণতি হতে পারে।
এটা মনে হতে পারে যে ফেজ ভারসাম্য একটি খালি বাক্যাংশ, এবং এই মুহুর্তে কয়েকটি শারীরিক প্রক্রিয়া রয়েছেজড়িত, কিন্তু, আমরা যেমন দেখেছি, এটি ছাড়া, আমাদের জানা অনেক আইন কাজ করে না, তাই আপনাকে এই অনন্য, রঙিন, যদিও কিছুটা বিরক্তিকর নিয়মগুলির সাথে একটু পরিচিত হতে হবে। এই জ্ঞান অনেক মানুষ সাহায্য করেছে. তারা শিখেছে কীভাবে সেগুলি নিজেদের উপর প্রয়োগ করতে হয়, উদাহরণস্বরূপ, ইলেকট্রিশিয়ান, পর্যায়ক্রমে কাজ করার নিয়মগুলি জেনে, অপ্রয়োজনীয় বিপদ থেকে নিজেদের রক্ষা করতে পারে৷






