পরিসংখ্যান ব্যবস্থায় ঘটে যাওয়া প্রক্রিয়াগুলি অধ্যয়ন করা কণার সর্বনিম্ন আকার এবং তাদের বিশাল সংখ্যার দ্বারা জটিল। প্রতিটি কণাকে আলাদাভাবে বিবেচনা করা কার্যত অসম্ভব, তাই পরিসংখ্যানগত পরিমাণ চালু করা হয়: কণার গড় গতি, তাদের ঘনত্ব, কণার ভর। মাইক্রোস্কোপিক পরামিতিগুলি বিবেচনায় নিয়ে সিস্টেমের অবস্থাকে চিহ্নিত করে এমন সূত্রটিকে গ্যাসের আণবিক-কাইনেটিক তত্ত্বের (MKT) মৌলিক সমীকরণ বলা হয়।
গড় কণার গতি সম্পর্কে কিছুটা
কণার গতি নির্ণয় প্রথম পরীক্ষামূলকভাবে করা হয়েছিল। অটো স্টার্ন দ্বারা পরিচালিত স্কুল পাঠ্যক্রমের একটি সুপরিচিত পরীক্ষা, কণার বেগের ধারণা তৈরি করা সম্ভব করেছে। পরীক্ষা চলাকালীন, ঘূর্ণায়মান সিলিন্ডারে রৌপ্য পরমাণুর গতি অধ্যয়ন করা হয়েছিল: প্রথমে, ইনস্টলেশনের একটি স্থির অবস্থায়, তারপর যখন এটি একটি নির্দিষ্ট কৌণিক বেগের সাথে ঘোরে।
ফলস্বরূপ, এটি পাওয়া গেছে যে রূপালী অণুর গতি শব্দের গতিকে ছাড়িয়ে গেছে এবং 500 মি/সেকেন্ড। ঘটনাটি বেশ মজার, যেহেতু একজন ব্যক্তির পক্ষে পদার্থে কণার চলাচলের গতি অনুভব করা কঠিন।
আদর্শ গ্যাস
গবেষণা চালিয়ে যানএটি কেবলমাত্র এমন একটি সিস্টেমে সম্ভব বলে মনে হয় যার পরামিতিগুলি শারীরিক যন্ত্র ব্যবহার করে সরাসরি পরিমাপ দ্বারা নির্ধারণ করা যেতে পারে। গতি একটি স্পিডোমিটার দিয়ে পরিমাপ করা হয়, তবে একটি কণার সাথে একটি স্পিডোমিটার সংযুক্ত করার ধারণাটি অযৌক্তিক। কণা গতির সাথে যুক্ত শুধুমাত্র একটি ম্যাক্রোস্কোপিক প্যারামিটার সরাসরি পরিমাপ করা যেতে পারে।
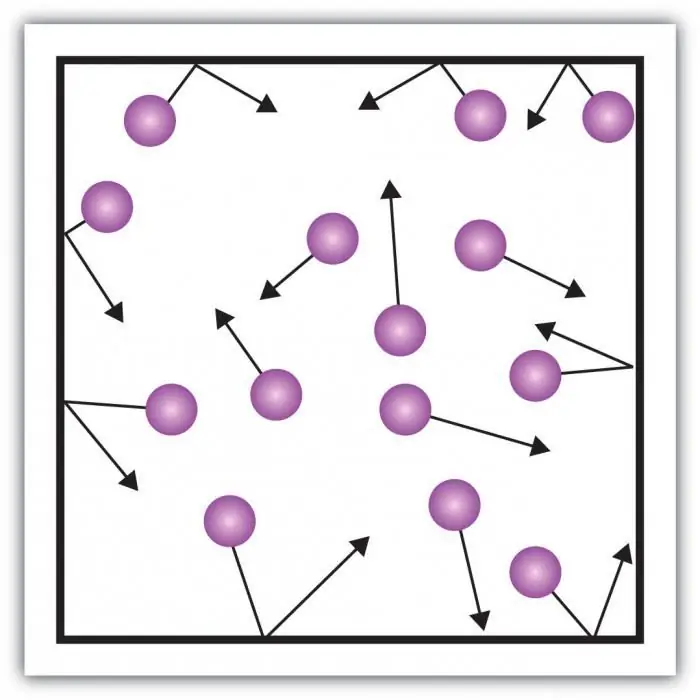
গ্যাসের চাপ বিবেচনা করুন। জাহাজের দেয়ালে চাপ তৈরি হয় জাহাজের গ্যাসের অণুর প্রভাবে। পদার্থের বায়বীয় অবস্থার বিশেষত্ব হল কণার মধ্যে যথেষ্ট বড় দূরত্ব এবং একে অপরের সাথে তাদের ছোট মিথস্ক্রিয়া। এটি আপনাকে সরাসরি এর চাপ পরিমাপ করতে দেয়৷
মিথস্ক্রিয়াকারী সংস্থাগুলির যে কোনও সিস্টেম সম্ভাব্য শক্তি এবং গতির গতিশক্তি দ্বারা চিহ্নিত করা হয়। বাস্তব গ্যাস একটি জটিল সিস্টেম। সম্ভাব্য শক্তির পরিবর্তনশীলতা পদ্ধতিগতকরণে নিজেকে ধার দেয় না। মিথস্ক্রিয়া জটিলতা একপাশে ঝাড়ু দিয়ে গ্যাসের বৈশিষ্ট্যযুক্ত বৈশিষ্ট্য বহন করে এমন একটি মডেল প্রবর্তন করে সমস্যার সমাধান করা যেতে পারে।
আদর্শ গ্যাস হল পদার্থের এমন একটি অবস্থা যেখানে কণার মিথস্ক্রিয়া নগণ্য, মিথস্ক্রিয়া সম্ভাব্য শক্তি শূন্যের দিকে ঝোঁক। শুধুমাত্র গতির শক্তি, যা কণার গতির উপর নির্ভর করে, তাৎপর্যপূর্ণ বলে বিবেচিত হতে পারে।
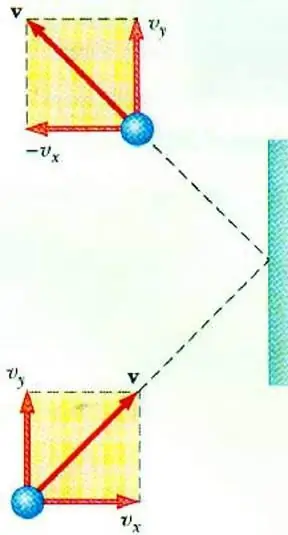
আদর্শ গ্যাসের চাপ
গ্যাসের চাপ এবং এর কণার গতির মধ্যে সম্পর্ক প্রকাশ করতে একটি আদর্শ গ্যাসের MKT এর মৌলিক সমীকরণের অনুমতি দেয়। একটি পাত্রে চলমান একটি কণা, দেয়ালের সাথে আঘাত করার পরে, এটিতে একটি আবেগ স্থানান্তরিত করে, যার মান দ্বিতীয় আইনের ভিত্তিতে নির্ধারণ করা যেতে পারেনিউটন:
F∆t=2m0vx
ইলাস্টিক প্রভাবের সময় একটি কণার ভরবেগের পরিবর্তন তার বেগের অনুভূমিক উপাদানের পরিবর্তনের সাথে সম্পর্কিত। F হল দেয়ালে কণার পাশ থেকে অল্প সময়ের জন্য ক্রিয়াশীল বল; m0- কণা ভর।
সমস্ত গ্যাস কণা ∆t সময়ে S এরিয়ার পৃষ্ঠের সাথে সংঘর্ষে লিপ্ত হয়, vx গতিতে পৃষ্ঠের দিকে চলে এবং Sυ আয়তনের একটি সিলিন্ডারে অবস্থিত x Δt. কণার ঘনত্ব n এ, ঠিক অর্ধেক অণু প্রাচীরের দিকে চলে যায়, বাকি অর্ধেক বিপরীত দিকে চলে যায়।
সমস্ত কণার সংঘর্ষ বিবেচনা করার পরে, আমরা এই অঞ্চলে ক্রিয়াশীল বলের জন্য নিউটনের সূত্র লিখতে পারি:
F∆t=nm0vx2S∆t
যেহেতু গ্যাসের চাপকে পরবর্তীটির ক্ষেত্রফলের সাথে পৃষ্ঠের লম্বভাবে কাজ করে এমন বলের অনুপাত হিসাবে সংজ্ঞায়িত করা হয়, আমরা লিখতে পারি:
p=F: S=nm0vx2
MKT-এর মৌলিক সমীকরণ হিসেবে প্রাপ্ত সম্পর্ক সমগ্র সিস্টেমকে বর্ণনা করতে পারে না, যেহেতু গতির একটি মাত্র দিক বিবেচনা করা হয়।
ম্যাক্সওয়েল বিতরণ
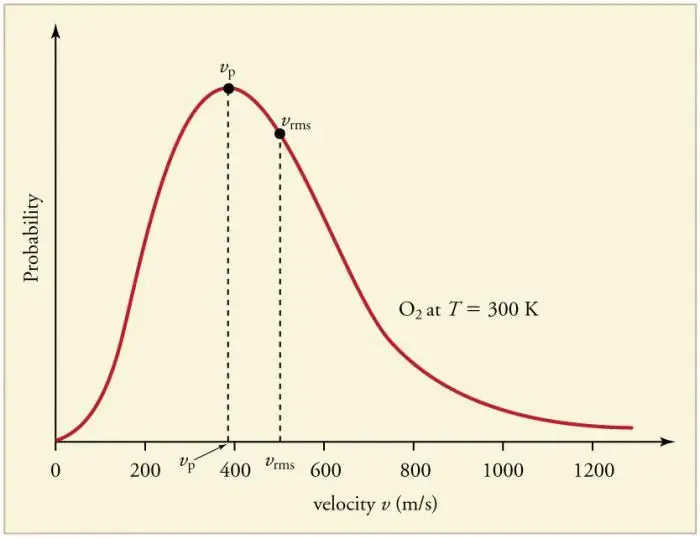
দেয়ালের সাথে এবং একে অপরের সাথে গ্যাস কণার ক্রমাগত ঘন ঘন সংঘর্ষ বেগের (শক্তি) পরিপ্রেক্ষিতে কণার একটি নির্দিষ্ট পরিসংখ্যানগত বন্টন প্রতিষ্ঠার দিকে পরিচালিত করে। সমস্ত বেগ ভেক্টরের দিকনির্দেশগুলি সমানভাবে সম্ভাব্য হতে দেখা যায়। এই বন্টনকে বলা হয় ম্যাক্সওয়েল ডিস্ট্রিবিউশন। 1860 সালে এই প্যাটার্ন ছিলMKT এর ভিত্তিতে জে ম্যাক্সওয়েল দ্বারা প্রাপ্ত। বণ্টন আইনের প্রধান পরামিতিগুলিকে বেগ বলা হয়: সম্ভাব্য, বক্ররেখার সর্বোচ্চ মানের সাথে সামঞ্জস্যপূর্ণ, এবং মূল-মান-বর্গ vkv=√‹v2 › - কণার বেগের গড় বর্গ।
গ্যাসের তাপমাত্রা বৃদ্ধি বেগের বৃদ্ধির সাথে মিলে যায়।
সকল গতি সমান, এবং তাদের মডিউলের মান একই, আমরা অনুমান করতে পারি:
‹v2›=‹vx2› + ‹v y2› + ‹vz2›, থেকে: ‹ vx2›=‹v2›: 3
MKT এর মৌলিক সমীকরণ, গ্যাসের চাপের গড় মান বিবেচনা করে, হল:
p=nm0‹v2›: 3.
এই সম্পর্কটি অনন্য যে এটি মাইক্রোস্কোপিক পরামিতিগুলির মধ্যে সম্পর্ক নির্ধারণ করে: গতি, কণার ভর, কণার ঘনত্ব এবং সাধারণভাবে গ্যাসের চাপ।
কণার গতিশক্তির ধারণা ব্যবহার করে, MKT-এর মৌলিক সমীকরণটি ভিন্নভাবে পুনরায় লেখা যেতে পারে:
p=2nm0‹v2›: 6=2n‹Ek>: 3
একটি গ্যাসের চাপ তার কণার গতিশক্তির গড় মানের সমানুপাতিক।
তাপমাত্রা
আশ্চর্যের বিষয় হল, একটি বন্ধ পাত্রে ধ্রুবক পরিমাণ গ্যাসের জন্য, কেউ গ্যাসের চাপ এবং কণা গতি শক্তির গড় মান সম্পর্কিত করতে পারে। এই ক্ষেত্রে, শক্তি পরিমাপ করে চাপ পরিমাপ করা যেতে পারেকণা।
কী করবেন? গতিশক্তির সাথে কোন মানকে তুলনা করা যায়? তাপমাত্রা এমন একটি মান হতে দেখা যাচ্ছে।

তাপমাত্রা হল পদার্থের তাপীয় অবস্থার পরিমাপ। এটি পরিমাপ করার জন্য, একটি থার্মোমিটার ব্যবহার করা হয়, যার ভিত্তিটি উত্তপ্ত হলে কার্যকরী তরল (অ্যালকোহল, পারদ) এর তাপীয় প্রসারণ। থার্মোমিটার স্কেল পরীক্ষামূলকভাবে তৈরি করা হয়। সাধারণত, একটি ধ্রুবক তাপীয় অবস্থায় (ফুটন্ত জল, বরফ গলে যাওয়া) কিছু শারীরিক প্রক্রিয়া চলাকালীন কার্যকারী তরলের অবস্থানের সাথে সঙ্গতিপূর্ণ চিহ্নগুলি স্থাপন করা হয়। বিভিন্ন থার্মোমিটারের বিভিন্ন স্কেল থাকে। উদাহরণস্বরূপ, সেলসিয়াস, ফারেনহাইট।

সর্বজনীন তাপমাত্রার স্কেল
গ্যাস থার্মোমিটারগুলি কার্যকারী তরলের বৈশিষ্ট্য থেকে স্বতন্ত্রতার ক্ষেত্রে আরও আকর্ষণীয় বলে বিবেচিত হতে পারে। তাদের স্কেল ব্যবহৃত গ্যাস ধরনের উপর নির্ভর করে না. এই ধরনের যন্ত্রে, যে তাপমাত্রায় গ্যাসের চাপ শূন্যের দিকে থাকে তা অনুমানিকভাবে এককভাবে বের করতে পারে। গণনা দেখায় যে এই মান -273.15 oC এর সাথে মিলে যায়৷ তাপমাত্রা স্কেল (পরম তাপমাত্রা স্কেল বা কেলভিন স্কেল) 1848 সালে চালু করা হয়েছিল। শূন্য গ্যাস চাপের সম্ভাব্য তাপমাত্রা এই স্কেলের প্রধান বিন্দু হিসাবে নেওয়া হয়েছিল। স্কেলের একটি ইউনিট সেগমেন্ট সেলসিয়াস স্কেলের একক মানের সমান। গ্যাস প্রক্রিয়া অধ্যয়ন করার সময় তাপমাত্রা ব্যবহার করে মৌলিক MKT সমীকরণটি লিখতে আরও সুবিধাজনক বলে মনে হয়।
চাপ এবং তাপমাত্রার মধ্যে সম্পর্ক
অভিজ্ঞতামূলকভাবে, আপনি এটি যাচাই করতে পারেনএর তাপমাত্রার সাথে গ্যাসের চাপের সমানুপাতিকতা। একই সময়ে, এটি পাওয়া গেছে যে চাপটি কণার ঘনত্বের সাথে সরাসরি সমানুপাতিক:
P=nkT,
যেখানে T পরম তাপমাত্রা, k একটি ধ্রুবক সমান 1.38•10-23J/K।
মৌলিক মান, যা সমস্ত গ্যাসের জন্য একটি ধ্রুবক মান রয়েছে, তাকে বোল্টজম্যান ধ্রুবক বলা হয়।
তাপমাত্রার উপর চাপের নির্ভরতা এবং MKT গ্যাসের মৌলিক সমীকরণের তুলনা করে আমরা লিখতে পারি:
‹Ek›=3kT: 2
গ্যাস অণুর গতিশীলতার গতিশক্তির গড় মান তার তাপমাত্রার সমানুপাতিক। অর্থাৎ, তাপমাত্রা কণা গতির গতিশক্তির পরিমাপ হিসাবে কাজ করতে পারে।






