তাপগতিবিদ্যা পদার্থবিদ্যার একটি গুরুত্বপূর্ণ শাখা। আমরা নিরাপদে বলতে পারি যে এর অর্জনগুলি প্রযুক্তিগত যুগের উত্থানের দিকে পরিচালিত করেছে এবং গত 300 বছরে মানব ইতিহাসের গতিপথ অনেকাংশে নির্ধারণ করেছে। নিবন্ধটি তাপগতিবিদ্যার প্রথম, দ্বিতীয় এবং তৃতীয় সূত্র এবং অনুশীলনে তাদের প্রয়োগ নিয়ে আলোচনা করে।
তাপগতিবিদ্যা কি?
থার্মোডাইনামিক্সের সূত্র তৈরি করার আগে, আসুন জেনে নেওয়া যাক পদার্থবিদ্যার এই বিভাগটি কী করে।
"তাপগতিবিদ্যা" শব্দটি গ্রীক উৎপত্তি এবং এর অর্থ "তাপের কারণে নড়াচড়া"। অর্থাৎ, পদার্থবিজ্ঞানের এই শাখাটি যেকোন প্রক্রিয়ার অধ্যয়নের সাথে জড়িত, যার ফলস্বরূপ তাপ শক্তি যান্ত্রিক গতিতে রূপান্তরিত হয় এবং এর বিপরীতে।
19 শতকের মাঝামাঝি তাপগতিবিদ্যার প্রাথমিক নিয়ম প্রণয়ন করা হয়েছিল। "আন্দোলন এবং তাপ" এর বিজ্ঞান পুরো সিস্টেমের আচরণকে সামগ্রিকভাবে বিবেচনা করে, এর ম্যাক্রোস্কোপিক পরামিতিগুলির পরিবর্তন অধ্যয়ন করে - তাপমাত্রা, চাপ এবং আয়তন, এবং এর মাইক্রোস্কোপিক কাঠামোর দিকে মনোযোগ না দেয়। তদুপরি, তাদের মধ্যে প্রথমটি আইন প্রণয়নে মৌলিক ভূমিকা পালন করেপদার্থবিদ্যায় তাপগতিবিদ্যা। এটা লক্ষ্য করা কৌতূহলী যে এগুলি শুধুমাত্র পরীক্ষামূলক পর্যবেক্ষণ থেকে উদ্ভূত হয়েছে৷
একটি থার্মোডাইনামিক সিস্টেমের ধারণা

এর অর্থ হল পরমাণু, অণু বা অন্যান্য উপাদানের যেকোন গোষ্ঠী যা সম্পূর্ণরূপে বিবেচিত হয়। তিনটি আইনই তথাকথিত থার্মোডাইনামিক সিস্টেমের জন্য প্রণীত। উদাহরণ হল: পৃথিবীর বায়ুমণ্ডল, কোনো জীবন্ত প্রাণী, একটি অভ্যন্তরীণ দহন ইঞ্জিনে গ্যাসের মিশ্রণ ইত্যাদি।
থার্মোডাইনামিক্সের সমস্ত সিস্টেম তিনটি প্রকারের একটির অন্তর্গত:
- খোলা। তারা পরিবেশের সাথে তাপ এবং পদার্থ উভয়ই বিনিময় করে। উদাহরণস্বরূপ, যদি খোলা আগুনে একটি পাত্রে খাবার রান্না করা হয়, তবে এটি একটি উন্মুক্ত ব্যবস্থার একটি উজ্জ্বল উদাহরণ, যেহেতু পাত্রটি বাহ্যিক পরিবেশ (আগুন) থেকে শক্তি গ্রহণ করে, যখন এটি নিজেই তাপের আকারে শক্তি বিকিরণ করে, এবং পানিও তা থেকে বাষ্পীভূত হয় (মেটাবলিজম)।
- বন্ধ। এই ধরনের সিস্টেমে পরিবেশের সাথে পদার্থের কোন বিনিময় হয় না, যদিও শক্তির বিনিময় ঘটে। পূর্ববর্তী ক্ষেত্রে ফিরে আসা: আপনি যদি কেটলিটিকে একটি ঢাকনা দিয়ে ঢেকে রাখেন তবে আপনি একটি বন্ধ সিস্টেম পেতে পারেন।
- বিচ্ছিন্ন। এটি এক ধরনের থার্মোডাইনামিক সিস্টেম যা পার্শ্ববর্তী স্থানের সাথে পদার্থ বা শক্তির বিনিময় করে না। একটি উদাহরণ হতে পারে একটি থার্মস যাতে গরম চা থাকে৷
থার্মোডাইনামিক তাপমাত্রা

এই ধারণার অর্থ হল আশেপাশের দেহ গঠনকারী কণাগুলির গতিশক্তি, যা গতি প্রতিফলিত করেকণার এলোমেলো আন্দোলন। এটি যত বড়, তাপমাত্রা তত বেশি। তদনুসারে, সিস্টেমের গতিশক্তি হ্রাস করে, আমরা এটিকে শীতল করি।
এই ধারণাটির অর্থ হল কণার গতিশক্তি যা আশেপাশের দেহ গঠন করে, যা কণার বিশৃঙ্খল গতিবিধির গতি প্রতিফলিত করে। এটি যত বড়, তাপমাত্রা তত বেশি। তদনুসারে, সিস্টেমের গতিশক্তি হ্রাস করে, আমরা এটিকে শীতল করি।
থার্মোডাইনামিক তাপমাত্রা কেলভিনের SI (ইন্টারন্যাশনাল সিস্টেম অফ ইউনিট) তে প্রকাশ করা হয় (ব্রিটিশ বিজ্ঞানী উইলিয়াম কেলভিনের সম্মানে, যিনি প্রথম এই স্কেলটি প্রস্তাব করেছিলেন)। তাপগতিবিদ্যার প্রথম, দ্বিতীয় এবং তৃতীয় সূত্র বোঝা তাপমাত্রার সংজ্ঞা ছাড়া অসম্ভব।
কেলভিন স্কেলে এক ডিগ্রির একটি বিভাজনও এক ডিগ্রি সেলসিয়াসের সাথে মিলে যায়। এই ইউনিটগুলির মধ্যে রূপান্তর সূত্র অনুসারে সঞ্চালিত হয়: TK =TC + 273, 15, যেখানে TK এবং TC - যথাক্রমে কেলভিন এবং ডিগ্রি সেলসিয়াসে তাপমাত্রা।
কেলভিন স্কেলের বিশেষত্ব হল এতে নেতিবাচক মান নেই। এতে শূন্য (TC=-273, 15 oC) সেই অবস্থার সাথে মিলে যায় যখন সিস্টেমের কণাগুলির তাপীয় গতি সম্পূর্ণ অনুপস্থিত থাকে, তারা "হিমায়িত" বলে মনে হচ্ছে।
শক্তির সংরক্ষণ এবং তাপগতিবিদ্যার ১ম সূত্র

1824 সালে, নিকোলাস লিওনার্ড সাদি কার্নোট, একজন ফরাসি প্রকৌশলী এবং পদার্থবিজ্ঞানী, একটি সাহসী পরামর্শ দিয়েছিলেন যা শুধুমাত্র পদার্থবিজ্ঞানের বিকাশের দিকে পরিচালিত করেনি, কিন্তু প্রযুক্তির উন্নতিতে একটি বড় পদক্ষেপও হয়ে ওঠে। তারনিম্নরূপ প্রণয়ন করা যেতে পারে: "শক্তি তৈরি বা ধ্বংস করা যায় না, এটি শুধুমাত্র এক রাজ্য থেকে অন্য রাজ্যে স্থানান্তরিত হতে পারে।"
আসলে, সাদি কার্নোটের বাক্যাংশটি শক্তির সংরক্ষণের আইনকে অনুমান করে, যা তাপগতিবিদ্যার ১ম সূত্রের ভিত্তি তৈরি করে: "যখনই একটি সিস্টেম বাইরে থেকে শক্তি গ্রহণ করে, তখনই এটিকে অন্য আকারে রূপান্তরিত করে, যার প্রধান যা তাপীয় এবং যান্ত্রিক।"
১ম আইনের গাণিতিক সূত্রটি নিম্নরূপ লেখা হয়েছে:
Q=ΔU + A, এখানে Q হল পরিবেশ দ্বারা সিস্টেমে স্থানান্তরিত তাপের পরিমাণ, ΔU হল এই সিস্টেমের অভ্যন্তরীণ শক্তির পরিবর্তন, A হল নিখুঁত যান্ত্রিক কাজ।
Adiabatic প্রক্রিয়া
এগুলির একটি ভাল উদাহরণ হল পর্বত ঢাল বরাবর বায়ু ভরের চলাচল। এই ধরনের ভর বিশাল (কিলোমিটার বা তার বেশি), এবং বায়ু একটি চমৎকার তাপ নিরোধক। উল্লিখিত বৈশিষ্ট্যগুলি আমাদেরকে বায়ুর ভরের সাথে যে কোনও প্রক্রিয়াকে অ্যাডিয়াব্যাটিক হিসাবে অল্প সময়ের মধ্যে বিবেচনা করার অনুমতি দেয়। যখন বায়ু পাহাড়ের ঢালে উঠে যায়, তখন তার চাপ কমে যায়, এটি প্রসারিত হয়, অর্থাৎ এটি যান্ত্রিক কাজ করে এবং ফলস্বরূপ, এটি শীতল হয়। বিপরীতে, বায়ুর ভরের নিম্নগামী চলাচলের সাথে এতে চাপ বৃদ্ধি পায়, এটি সংকুচিত হয় এবং এর কারণে, খুব গরম হয়ে যায়।
তাপগতিবিদ্যার আইনের প্রয়োগ, যা পূর্ববর্তী উপশিরোনামে আলোচনা করা হয়েছিল, এটি একটি adiabatic প্রক্রিয়ার উদাহরণ ব্যবহার করে সবচেয়ে সহজে প্রদর্শিত হয়৷
সংজ্ঞা অনুসারে, এর ফলে এর সাথে শক্তির কোনও বিনিময় হয় নাপরিবেশ, অর্থাৎ, উপরের সমীকরণে, Q=0। এটি নিম্নলিখিত অভিব্যক্তির দিকে নিয়ে যায়: ΔU=-A। এখানে বিয়োগ চিহ্নের অর্থ হল সিস্টেমটি তার নিজস্ব অভ্যন্তরীণ শক্তি হ্রাস করে যান্ত্রিক কাজ করে। এটা মনে রাখা উচিত যে অভ্যন্তরীণ শক্তি সরাসরি সিস্টেমের তাপমাত্রার উপর নির্ভরশীল।
থার্মাল প্রসেসের দিকনির্দেশ
এই সমস্যাটি তাপগতিবিদ্যার ২য় সূত্রের সাথে সম্পর্কিত। অবশ্যই সবাই লক্ষ্য করেছেন যে আপনি যদি ভিন্ন তাপমাত্রার দুটি বস্তুকে সংস্পর্শে আনেন, তবে ঠান্ডাটি সর্বদা উত্তপ্ত হবে এবং গরমটি শীতল হবে। উল্লেখ্য যে বিপরীত প্রক্রিয়াটি তাপগতিবিদ্যার প্রথম সূত্রের কাঠামোর মধ্যে ঘটতে পারে, কিন্তু বাস্তবে তা কখনই বাস্তবায়িত হয় না।
এই প্রক্রিয়াটির অপরিবর্তনীয়তার কারণ (এবং মহাবিশ্বের সমস্ত পরিচিত প্রক্রিয়া) হল সিস্টেমের একটি আরও সম্ভাব্য অবস্থায় রূপান্তর। বিবেচিত উদাহরণে ভিন্ন তাপমাত্রার দুটি বস্তুর সংস্পর্শে, সবচেয়ে সম্ভাব্য অবস্থা হবে এমন একটি যেখানে সিস্টেমের সমস্ত কণার গতিশক্তি একই থাকবে।
তাপগতিবিদ্যার দ্বিতীয় সূত্রটি নিম্নরূপ প্রণয়ন করা যেতে পারে: "তাপ কখনই স্বতঃস্ফূর্তভাবে ঠান্ডা শরীর থেকে গরমে স্থানান্তরিত হতে পারে না।" যদি আমরা ব্যাধির পরিমাপ হিসাবে এনট্রপির ধারণাটি প্রবর্তন করি, তবে এটিকে নিম্নরূপ উপস্থাপন করা যেতে পারে: "যেকোনো তাপগতি প্রক্রিয়া এনট্রপি বৃদ্ধির সাথে এগিয়ে যায়"
হিট ইঞ্জিন

এই শব্দটি এমন একটি সিস্টেম হিসাবে বোঝা যায় যা, এটিতে বাহ্যিক শক্তি সরবরাহের কারণে, যান্ত্রিক কাজ সম্পাদন করতে পারে। প্রথমতাপ ইঞ্জিনগুলি ছিল বাষ্পীয় ইঞ্জিন এবং 17 শতকের শেষে উদ্ভাবিত হয়েছিল৷
তাপগতিবিদ্যার দ্বিতীয় সূত্রটি তাদের কার্যকারিতা নির্ধারণে একটি নির্ধারক ভূমিকা পালন করে। সাদি কার্নোট আরও প্রতিষ্ঠিত করেছেন যে এই ডিভাইসের সর্বাধিক কার্যকারিতা হল: দক্ষতা=(T2 - T1)/T2, এখানে T2 এবং T1 হিটার এবং রেফ্রিজারেটরের তাপমাত্রা। যান্ত্রিক কাজ তখনই করা যেতে পারে যখন গরম শরীর থেকে ঠান্ডা শরীরে তাপের প্রবাহ থাকে এবং এই প্রবাহকে 100% দরকারী শক্তিতে রূপান্তরিত করা যায় না।
নীচের চিত্রটি একটি তাপ ইঞ্জিনের পরিচালনার নীতি দেখায় (Qabs - মেশিনে তাপ স্থানান্তরিত হয়, Qced - তাপ হ্রাস, W - দরকারী কাজ, P এবং V - পিস্টনে গ্যাসের চাপ এবং আয়তন)।
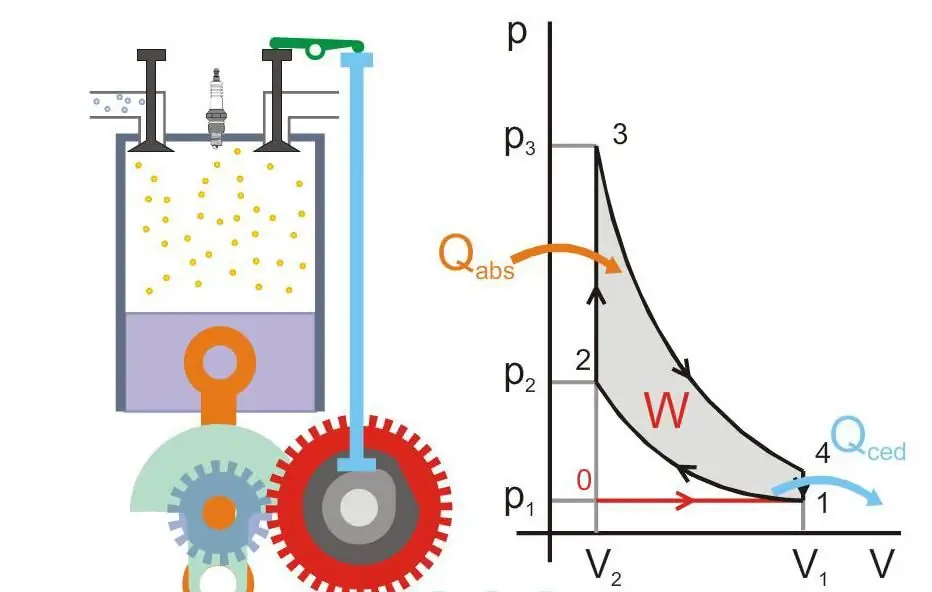
পরম শূন্য এবং নার্নস্টের অনুমান
অবশেষে, তাপগতিবিদ্যার তৃতীয় সূত্রের বিবেচনায় এগিয়ে যাওয়া যাক। একে Nernst postulate (জার্মান পদার্থবিজ্ঞানীর নাম যিনি 20 শতকের শুরুতে এটি প্রথম প্রণয়ন করেছিলেন) নামেও পরিচিত। আইন বলে: "একটি সীমিত সংখ্যক প্রক্রিয়ার মাধ্যমে পরম শূন্যে পৌঁছানো যায় না।" অর্থাৎ, কোনো পদার্থের অণু এবং পরমাণুকে সম্পূর্ণরূপে "হিমায়িত" করা কোনোভাবেই অসম্ভব। এর কারণ হল পরিবেশের সাথে অবিরাম বিদ্যমান তাপ বিনিময়।

থার্মোডাইনামিক্সের তৃতীয় সূত্র থেকে একটি দরকারী উপসংহার টানা হল যে এনট্রপি যখন পরম শূন্যের দিকে যায় তখন কমে যায়। এর মানে হল যে সিস্টেমটি নিজেকে সংগঠিত করার প্রবণতা রাখে। এই বাস্তবতা পারেউদাহরণস্বরূপ, প্যারাম্যাগনেটগুলিকে ঠাণ্ডা হলে ফেরোম্যাগনেটিক অবস্থায় স্থানান্তর করতে ব্যবহার করুন।
এটি লক্ষ্য করা আকর্ষণীয় যে এখন পর্যন্ত সর্বনিম্ন তাপমাত্রা 5·10−10 K (2003, MIT ল্যাবরেটরি, USA)।






