আণবিক-কাইনেটিক তত্ত্ব, সিস্টেমের মাইক্রোস্কোপিক আচরণ বিশ্লেষণ করে এবং পরিসংখ্যানগত বলবিদ্যার পদ্ধতি ব্যবহার করে তাপগতিগত সিস্টেমের গুরুত্বপূর্ণ ম্যাক্রোস্কোপিক বৈশিষ্ট্যগুলি পেতে দেয়। মাইক্রোস্কোপিক বৈশিষ্ট্যগুলির মধ্যে একটি, যা সিস্টেমের তাপমাত্রার সাথে সম্পর্কিত, গ্যাস অণুর গড় বর্গ বেগ। আমরা এটির সূত্র দিই এবং নিবন্ধে এটি বিবেচনা করি৷
আদর্শ গ্যাস
আমরা এখনই লক্ষ্য করি যে গ্যাসের অণুর দ্বিঘাত গড় বেগের সূত্রটি একটি আদর্শ গ্যাসের জন্য বিশেষভাবে দেওয়া হবে। এর অধীনে, পদার্থবিজ্ঞানে, এমন একটি বহু-কণা ব্যবস্থা বিবেচনা করা হয় যেখানে কণাগুলি (পরমাণু, অণু) একে অপরের সাথে মিথস্ক্রিয়া করে না (তাদের গতিশক্তি বিভিন্ন মাত্রার ক্রিয়াকলাপের সম্ভাব্য শক্তিকে অতিক্রম করে) এবং মাত্রা নেই, অর্থাৎ, তারা একটি সীমিত ভর সহ বিন্দু (কণার মধ্যে দূরত্ব তাদের আকারের চেয়ে অনেক বেশি মাত্রার ক্রম।রৈখিক)।
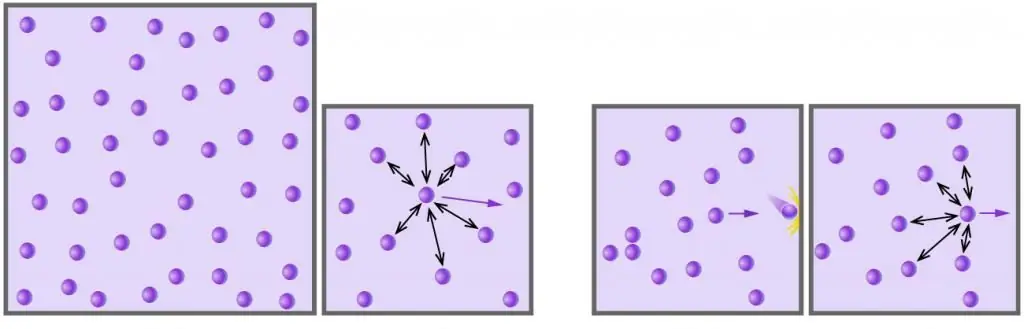
যেকোন গ্যাস যা রাসায়নিকভাবে নিরপেক্ষ অণু বা পরমাণু নিয়ে গঠিত এবং যেটি নিম্নচাপের মধ্যে থাকে এবং উচ্চ তাপমাত্রা থাকে, তাকে আদর্শ হিসাবে বিবেচনা করা যেতে পারে। উদাহরণস্বরূপ, বায়ু একটি আদর্শ গ্যাস, কিন্তু জলীয় বাষ্প আর তেমন নেই (জলীয় হাইড্রোজেন বন্ধন জলের অণুর মধ্যে কাজ করে)।
আণবিক গতি তত্ত্ব (MKT)

MKT এর কাঠামোর মধ্যে একটি আদর্শ গ্যাস অধ্যয়ন করার জন্য, আপনার দুটি গুরুত্বপূর্ণ প্রক্রিয়াগুলিতে মনোযোগ দেওয়া উচিত:
- গ্যাস এটি ধারণ করা জাহাজের দেয়ালে স্থানান্তর করে চাপ সৃষ্টি করে, যখন অণু এবং পরমাণু তাদের সাথে সংঘর্ষ হয়। এই ধরনের সংঘর্ষ পুরোপুরি স্থিতিস্থাপক৷
- গ্যাসের অণু এবং পরমাণু বিভিন্ন বেগের সাথে সব দিকে এলোমেলোভাবে চলে, যার বন্টন ম্যাক্সওয়েল-বোল্টজম্যান পরিসংখ্যান মেনে চলে। কণাগুলির মধ্যে সংঘর্ষের সম্ভাবনা অত্যন্ত কম, কারণ তাদের আকার নগণ্য এবং তাদের মধ্যে বড় দূরত্ব৷
গ্যাস কণার স্বতন্ত্র গতি একে অপরের থেকে খুব আলাদা হওয়া সত্ত্বেও, সিস্টেমে কোনও বাহ্যিক প্রভাব না থাকলে এই মানের গড় মান সময়ের সাথে স্থির থাকে। গতিশক্তি এবং তাপমাত্রার মধ্যে সম্পর্ক বিবেচনা করে গ্যাসের অণুর গড় বর্গ বেগের সূত্রটি পাওয়া যেতে পারে। আমরা নিবন্ধের পরবর্তী অনুচ্ছেদে এই সমস্যাটি মোকাবেলা করব৷
আদর্শ গ্যাস অণুর দ্বিঘাত গড় বেগের জন্য সূত্রের প্রাপ্তি
প্রত্যেক শিক্ষার্থী পদার্থবিদ্যার সাধারণ পাঠক্রম থেকে জানে যে m ভর সহ একটি শরীরের অনুবাদমূলক গতির গতিশক্তি নিম্নরূপ গণনা করা হয়:
Ek=mv2/2
যেখানে v রৈখিক গতি। অন্যদিকে, রূপান্তর ফ্যাক্টর kB(বোল্টজম্যানের ধ্রুবক) ব্যবহার করে একটি কণার গতিশক্তিও পরম তাপমাত্রা T এর পরিপ্রেক্ষিতে নির্ধারণ করা যেতে পারে। যেহেতু আমাদের স্থান ত্রিমাত্রিক, তাই Ek নিম্নরূপ গণনা করা হয়:
Ek=3/2kBT.
সমতা উভয়ের সমান এবং তাদের থেকে v প্রকাশ করলে, আমরা একটি দ্বিঘাত আদর্শ গ্যাসের গড় বেগের সূত্রটি পাই:
mv2/2=3/2kBT=>
v=√(3kBT/m)।
এই সূত্রে, m - গ্যাস কণার ভর। এর মান ব্যবহারিক গণনায় ব্যবহার করা অসুবিধাজনক, কারণ এটি ছোট (≈ 10-27kg)। এই অসুবিধা এড়াতে, আসুন আমরা সর্বজনীন গ্যাস ধ্রুবক R এবং মোলার ভর M স্মরণ করি। kB এর সাথে ধ্রুবক R সমতার সাথে সম্পর্কিত:
kB=R/NA।
M এর মান নিম্নরূপ সংজ্ঞায়িত করা হয়েছে:
M=mNA.
উভয় সমতা বিবেচনায় রেখে, আমরা অণুর মূল-গড়-বর্গ বেগের জন্য নিম্নলিখিত অভিব্যক্তিটি পাই:
v=√(3RT/M)।
এইভাবে, গ্যাস কণার গড় বর্গ বেগ পরম তাপমাত্রার বর্গমূলের সরাসরি সমানুপাতিক এবং মোলার ভরের বর্গমূলের বিপরীতভাবে সমানুপাতিক৷
সমস্যা সমাধানের উদাহরণ
সবাই জানে যে আমরা যে বাতাসে শ্বাস নিই তা 99% নাইট্রোজেন এবং অক্সিজেন। N2 এবং O2 15 o তাপমাত্রায় অণুর গড় বেগের পার্থক্য নির্ধারণ করা প্রয়োজন। C.

এই সমস্যাটি পর্যায়ক্রমে সমাধান করা হবে। প্রথমত, আমরা তাপমাত্রাকে পরম এককে অনুবাদ করি, আমাদের আছে:
T=273, 15 + 15=288, 15 K.
এখন বিবেচনাধীন প্রতিটি অণুর জন্য মোলার ভর লিখুন:
MN2=0.028 kg/mol;
MO2=0.032 kg/mol.
যেহেতু মোলার ভরের মান কিছুটা আলাদা, একই তাপমাত্রায় তাদের গড় গতিও কাছাকাছি হওয়া উচিত। v এর সূত্র ব্যবহার করে, আমরা নাইট্রোজেন এবং অক্সিজেন অণুর জন্য নিম্নলিখিত মানগুলি পাই:
v (N2)=√(38, 314288, 15/0, 028)=506.6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473.9 m/s.
নাইট্রোজেন অণু অক্সিজেন অণুর তুলনায় সামান্য হালকা হওয়ার কারণে তারা দ্রুত চলে। গড় গতির পার্থক্য হল:
v (N2) - v (O2)=506.6 - 473.9=32.7 m/s.
ফলিত মান নাইট্রোজেন অণুর গড় গতির মাত্র 6.5%। আমরা গ্যাসে অণুর উচ্চ বেগের দিকে দৃষ্টি আকর্ষণ করি, এমনকি নিম্ন তাপমাত্রায়ও।






